题目内容
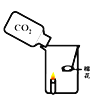
【题目】在今年五校“庆元旦 贺新年”联欢晚会上,戴校长给同学们表演了一个魔术:大烧杯中盛有一只燃着的蜡烛和一团包有过氧化钠(Na2O2)的棉花,将一瓶二氧化碳倒入烧杯中,蜡烛慢慢的熄灭,然后棉花突然剧烈的燃烧起来。这出乎意料的现象引起了同学们的极大兴趣,请你参与同学们的讨论和探究。
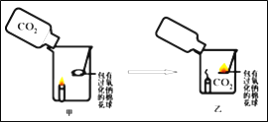
蜡烛熄灭的原因是___________________________。
(提出问题)棉花为什么会燃烧?
(提出猜想)
(1)可能是蜡烛燃烧引燃了棉花。
(2)可能是二氧化碳与过氧化钠反应生成了氧气。
(3)______________________________________。
(实验验证)
序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
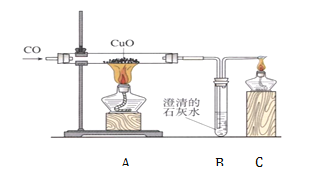
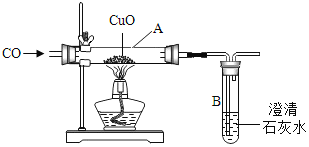
① | 按下图装置进行实验
| 蜡烛慢慢熄灭 | 猜想﹙1﹚___ ﹙填成立或不成立﹚ |
② | 向盛满二氧化碳的氧气瓶中进入适量的过氧化钠粉末,成分震荡,并______ | _________ | 二氧化碳与过氧化钠反应生成了氧气猜想﹙2﹚成立 |
③ | _____________ | _________ | 猜想﹙3﹚成立 |
(实验结论)
(1)CO2 与Na2O2反应生成了氧气与一种化合物,化学方程式为_________________。
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。
【答案】与氧气隔绝 可能是过氧化钠与二氧化碳反应放出热量,引燃了棉花 不成立 将带火星的木条伸入集气瓶中 带火星的木条复燃 向盛满CO2的集气瓶中加入适量Na2O2 用手触摸瓶壁 ,瓶壁温度升高 2Na2O2+2CO2===2Na2CO3+O2
【解析】
(1)蜡烛熄灭的根本原因是烧杯中倒入二氧化碳后,与氧气隔绝;【提出猜想】从过氧化钠和二氧化碳反应考虑:可能是过氧化钠与二氧化碳反应放出热量,引燃了棉花
【实验验证】猜想①中探究的是:可能是蜡烛燃烧引燃了棉花。所示装置进行实验,点燃蜡烛,慢慢熄灭,猜想一不成立;猜想②向盛满二氧化碳的集气瓶中加入适量的过氧化钠粉末,充分振荡,并将带火星的木条伸入集气瓶中,带火星的木条复燃。可知二氧化碳与过氧化
钠反应生成了氧气;猜想③向盛满二氧化碳的集气瓶中撒入适量过氧化钠,用手触摸瓶壁,发现瓶壁温度升高,说明反应放热,故猜想③成立;【实验结论】(1)CO2 与Na2O2反应生成了氧气与一种化合物,化学方程式为:2Na2O2+2CO2===2Na2CO3+O2。

【题目】有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应)。课外小组为了测定该石灰石样品中碳酸钙的质量分数,将一定量的石灰石样品放入烧杯中,再将100 g稀盐酸分4次加入烧杯中,每次均充分反应。实验数据记录如下:
次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
反应后烧杯中物质的总质量/g | 35.2 | 58.4 | 82.6 | 107.6 |
(1)第1次加入稀盐酸充分反应后,生成二氧化碳的质量。
(2)该石灰石样品中碳酸钙的质量。