题目内容
【题目】金属在生产生活中起着重要作用。
(1)对Ag、Fe、Cu 三种金属活动性顺序的探究,下列所选试剂组不可行的是________________。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
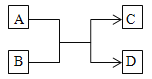
(2)化学小组在实验结束后,进行了如下废液处理:
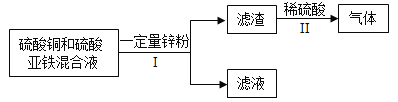
①写出Ⅱ中一定发生反应的化学方程式________________。
②滤液的组成可能是________________。
【答案】② ![]() 硫酸锌或硫酸锌和硫酸亚铁
硫酸锌或硫酸锌和硫酸亚铁
【解析】
(1)①Fe、Ag、CuSO4溶液这三种物质中,Fe与CuSO4溶液反应,证明铁的活动性比铜强,Ag与CuSO4溶液不能反应,证明铜比银的活动性强。所以,可以证明活动性由强到弱为铁、铜、银。所选试剂组可行;
②因为铁的活动性在三种金属中最强,所以Cu,Ag都不能和FeSO4溶液反应,得不出Cu,Ag的活动性强弱,所以此试剂组不可行;
③Cu、FeSO4溶液、AgNO3溶液这三种物质中,Cu与FeSO4溶液不反应,证明铁的活动性比铜强,Cu与AgNO3溶液能反应,证明铜比银的活动性强,可以证明活动性由强到弱为铁、铜、银,此试剂组可行。故选②。
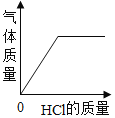
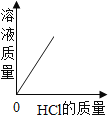
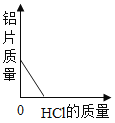
(2)金属活动性由强到弱为锌、铁、铜,锌先和硫酸铜反应生成硫酸锌和铜,再和硫酸亚铁反应生成硫酸锌和铁。滤渣能和稀硫酸反应生成气体,则滤渣中有铁或锌、铁(如果锌过量,则滤渣中含有铁和锌,如果锌不足或恰好反应,则滤渣中只含有铁)。因此Ⅱ中一定发生反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑。
②如果锌过量,则滤液是硫酸锌溶液,如果锌不足,则滤液是硫酸锌溶液和硫酸亚铁溶液。

【题目】研究金属的腐蚀对资源的利用和保护意义重大。
(1)为了探究铁锈蚀的条件,进行如图-12所示实验。经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。

①通过实验发现:铁锈蚀是铁与_____________发生化学反应的过程。
② A中加入的蒸馏水要事先煮沸,其目的是______________________。
(2)家中的刀具若沾有食盐水锈蚀更快。为了进一步探究影响铁锈蚀速率的因素,做了如下的实验。
(提出问题)铁锈蚀速率与哪些因素有关。
(查阅资料)①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液。
②氯化钠溶液能导电;乙醇溶液不能导电。
(猜想)铁的锈蚀速率与下列因素有关:
①反应时的温度;②氧气的含量;③水溶液的导电性。
(实验)每次取两套如图-13所示的装置,编号为I、II。向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致)。

影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中。 | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II。 | 锈蚀的速率I<II;铁的锈蚀速率与反应时的温度有关,_。 |
②氧气含量 |
|
| 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快。 |
③水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇。 | 两套装置中铁钉均锈蚀; |
|
(3)若将两根铁钉分别放入两支试管中,在一支试管中加入稀硫酸,另一支试管中加入稀盐酸,观察到两支试管内均有大量气泡产生,铁钉逐渐溶解,在酸溶液中被快速腐蚀。
(反思与提高)
根据该探究实验以及你所学的知识,判断下列说法正确的是________(填序号)。
A金属的腐蚀是指金属单质与其它物质发生化学反应的过程[
B金属越活泼,就越容易被锈蚀
C金属腐蚀不一定要有氧气参加