题目内容
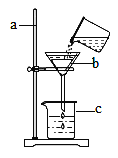
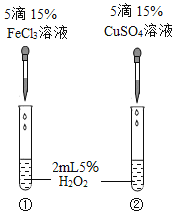
【题目】为比较Fe3+和Cu2+对过氧化氢分解反应的催化效果,某同学设计了如图所示的实验(FeCl3溶液、CuSO4溶液中都含有阴阳离子和水分子),有关实验有如下说法:
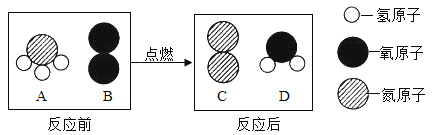
①过氧化氢中氧元素的化合价为-1价;
②若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好;
③实验中可通过观察产生气泡快慢来比较反应速率;
④滴加FeCl3或CuSO4溶液后过氧化氢分解速率加快,则FeCl3或CuSO4是过氧化氢催化剂
以上说法不正确的是( )
A.①②B.①④C.②④D.③④
【答案】C
【解析】
①过氧化氢中氢显+1价,根据化合物中元素化合价之和为零,可知氧元素的化合价为-1价,故①正确;
②因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,故②错误;
③反应的剧烈程度与实验现象有关,反应越剧烈,产生气体的速率越快,产生气泡越快,故③正确;
④证明氯化铁或硫酸铜是过氧化氢分解的催化剂,还需要验证质量和化学性质不变,故④错误。所以说法不正确的是②④。故选C。

 培优好卷单元加期末卷系列答案
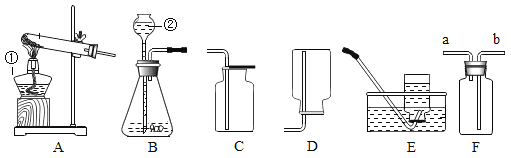
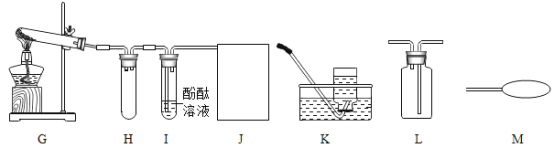
培优好卷单元加期末卷系列答案【题目】如图为实验室制取气体的常见装置:
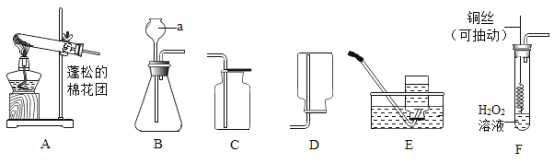
(1)制取和收集气体:任意写出一个实验室制氧气的化学方程式_____.利用该装置制氧气的发生装置为_____(选填“A ””B”)收集装置为_____(“C”“D”“E”),实验室制取二氧化碳的方程式为_____.
(2)实验改进:查阅资料发现,氧化铜可以做过氧化氢制氧气的催化剂,现有一根洁净的铜丝,实验前先绕成螺旋状,再经_____处理,改进后装置如图F所示,铜丝绕成螺旋状的目的是_____,将铜丝换成铜制的网兜,与改进前装置相比,改进后共同的优点是_____.
(3)温度、浓度、固体的颗粒大小等因素会影响反应速率.为研究实验室制取二氧化碳的适宜条件,进行如表四组实验:
实验编号药品 | 甲 | 乙 | 丙 | 丁 |
mg大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
mg验算(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
①实验甲与_____对照(填编号),是为了研究固体反应物颗粒大小对反应速率的影响;
②上述实验中,另一个影响反应速率的因素是_____.