题目内容
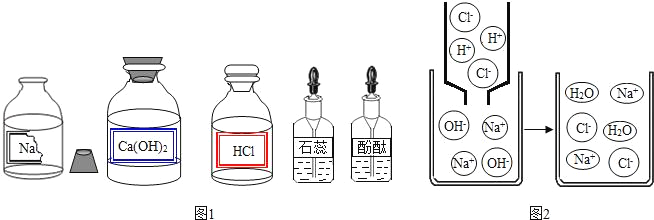
【题目】某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图1),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
(提出问题)这瓶溶液是什么溶液?
(获得信息)酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
(提出猜想)这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;
猜想三:碳酸钠溶液.
(实验推断)
(1)小丽取样滴加无色酚酞试液,溶液呈红色,得出结论:该溶液不可能是_____溶液,理由是_____;
(2)小刚另取样滴加稀盐酸有_____产生,反应的化学方程式为_____,小刚得出结论:该溶液是碳酸钠溶液.
(3)小青认为小刚的结论不完全正确,理由是_____.
小组同学讨论后一致认为还需要进行如下实验:
(继续探究)另取样加入过量的CaCl2溶液,观察到有_____产生,设计这一步骤的目的是_____;静置后,取上层清液,滴入酚酞试液,溶液呈红色.
(实验结论)这瓶溶液是_____.
(探究启示)实验取完药品后应_____.
(拓展迁移)若该溶液与盐酸发生中和反应,恰好完全反应的微观过程如右图所示,反应的实质表达式为: H++OH﹣═H2O,则反应后溶液中存在的阴、阳离子是_____(填符号).
【答案】氯化钠 氯化钠溶液呈中性 气泡 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 氢氧化钠能与二氧化碳反应生成碳酸钠 白色沉淀 除去碳酸钠,防止干扰 氢氧化钠和碳酸钠 立即盖上瓶盖 Na+、Cl﹣
【解析】
(1)氢氧化钠和碳酸钠溶液都呈碱性能使酚酞试液变红色,氯化钠溶液呈中性,所以,小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液;
(2)若有碳酸钠存在,滴加盐酸,发生反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,有气泡产生.所以,小刚另取样滴加稀盐酸有气泡产生,小刚得出结论:该溶液是碳酸钠溶液;
(3)因为该试剂是敞口放置于空气中,若是氢氧化钠可能会和空气中二氧化碳反应变质生成部分碳酸钠,所以,小青认为小刚的结论不完全正确,理由是露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠.
【继续探究】
要证明原来是氢氧化钠,可先加过量的氯化钡或氯化钙溶液溶液除尽碳酸根,再用酚酞检验氢氧化钠的存在.所以,另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是完全除去溶液中的CO32﹣,避免其对OH﹣检验造成干扰;静置后,取上层清液,滴入酚酞试液,溶液呈红色;
【实验结论】
因为滴加氯化钙有白色沉淀产生且,滴加酚酞变红色,说明溶液中含有碳酸钠和氢氧化钠;
【探究启示】
由于氢氧化钠易与空气中的二氧化碳反应,所以,实验取完药品后应立即盖好瓶盖;
【拓展迁移】
通过观察反应的微观过程图,可以看出反应后溶液的阴阳离子为Cl﹣、Na+.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】除杂是化学中重要的实验操作,下列除杂所用试剂和操作完全错误的一组是( )
物质 | 杂质 | 除杂所用试剂或方法 | |
A | CO2 | O2 | 通过灼热的碳层 |
B | FeSO4 | CuSO4 | 加入过量的铁粉,过滤 |
C | CO | CO2 | 通过足量的石灰水 |
D | CaO | CaCO3 | 高温煅烧 |
A. AB. BC. CD. D
【题目】某校化学兴趣小组在查阅资料中发现:可燃物燃烧需要的最低氧含量数据如表:
请结合数据回答下列问题:
可燃物名称 | 蜡烛 | 木炭 | 棉花 | 红磷 | 白磷 |
最低氧含量/% | 16 | 14 | 8 | 8.8 | 3.2 |
(1)图1为教材中测量空气中氧气体积分数的实验装置图:请写出集气瓶中发生的反应的化学方程式:______结合数据,你认为红磷适合于测量空气中氧气的体积分数吗?你的理由是:______。但实验过程中又确实看到进来的水的体积约占集气瓶内容积的![]() .其原因可能是:______。
.其原因可能是:______。
(2)图2是拉瓦锡的实验装置,回看拉瓦锡的实验选择汞的优点有:______(不定项选择)
A.实验过程没有污染
B.在汞槽中起到液封作用
C.生成的化合物加热分解后又得到汞和氧气
D.能将密闭装置内空气中的氧气几乎耗尽
(3)请你结合数据设计一个实验证明密闭装置内红磷熄灭后的空气中还有氧气,写出操作步骤和现象:______。
(4)已知当氧气浓度为10%﹣14%时,人仍有意识,但会出现判断失误,且本身不察觉。当氧气浓度为6%﹣8%时,人会呼吸停止,并在68分钟内死亡。所以为进入某储藏蔬菜的地窖,一般都会进行灯火实验,结合数据分析使用蜡烛做灯火实验可靠吗?并说明理由:______。