题目内容
【题目】除杂是化学中重要的实验操作,下列除杂所用试剂和操作完全错误的一组是( )
物质 | 杂质 | 除杂所用试剂或方法 | |
A | CO2 | O2 | 通过灼热的碳层 |
B | FeSO4 | CuSO4 | 加入过量的铁粉,过滤 |
C | CO | CO2 | 通过足量的石灰水 |
D | CaO | CaCO3 | 高温煅烧 |
A. AB. BC. CD. D
【答案】A
【解析】
A、CO2中混有杂质O2,通过灼热的碳层不可行,因为二氧化碳、氧气都能与碳反应,此选项错误;
B、FeSO4中混有杂质CuSO4,加入过量的铁粉,Fe+CuSO4 ==Cu+FeSO4 ,过滤,将固体物质滤出,得到FeSO4,此选项正确;
C、CO中混有杂质CO2,通过足量的石灰水可除去,CO2+Ca(OH)2==CaCO3↓+H2O,此选项正确;
D、CaO中混有杂质CaCO3,高温煅烧可行,CaCO3![]() CaO+CO2↑,此选项正确。故选A。
CaO+CO2↑,此选项正确。故选A。

【题目】根据题意填空:
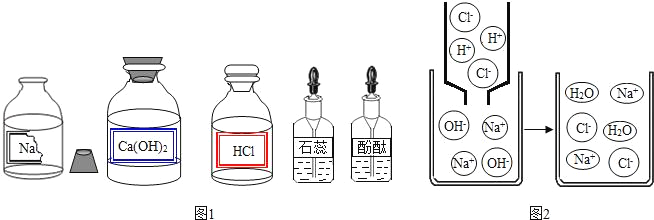
(1)用化学符号表示下列图片中信息,其中“O”表示氢原子,“●”表示氮原子。
图片 |
|
|
|
|
符号 | ______ | ______ | ______ | ______ |
(2)保持水的化学性质的是______(填化学符号);
(3)氯化钠是由______构成(填微粒名称)
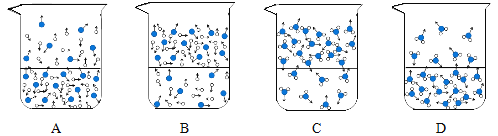
(4)下列图示能反映水在空气中放置时发生变化的微观示意图是______(填字母序号)。(图中“●”表示氧原子,“o”表示氢原子)
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物 1~2.5g进行系列实验。
(查阅资料)①碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;
②氧化亚铜为红色固体,能与稀硫酸反应:
Cu2O+H2SO4=CuSO4+H2O+Cu。
(进行实验)
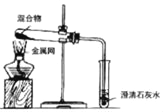
实验 1:取质量比 1:11 的木炭粉和氧化铜混合物 1.3g,进行实验。
序号 | 1﹣1 | 1﹣2 |
装置 |
|
|
反 应 后 物 质 的颜色、状态 | 黑色粉末中混有少量红色固体。 | 红色固体有金属光泽,混有 极少量黑色物质。 |
实验 2:取一定量的混合物,用 1﹣2 装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2﹣1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2﹣2 | 1:10 | 混有很少量黑色物质 | |
2﹣3 | 1:11 | 混有极少量黑色物质 | |
2﹣4 | 1:12 | 无黑色物质 | |
2﹣5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
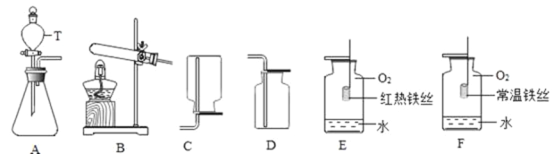
(1)实验中酒精灯火焰处罩金属网的作用:_____;
(2)加热试管中的固体,一般试管口要向_____倾斜,但在实验 1﹣2 中试管却可以 垂直向上放置,这是因为_____;
(3)实验 1﹣2 中,证明产生了 CO2 的现象是_____;
(4)实验 2 的结论是_____;
(反思与评价)
(5)实验 2 没有进行质量比为 1:14 的实验,理由是_____;
(6)为检验 2﹣4 的红色固体中是否含 Cu2O,所需试剂是_____。
(7)实验改进的思路和方法很多,本题是从_____的设计和_____的控制两个方面的改进来达到实验效果的最优化。