题目内容
【题目】A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、二氧化碳中的一种,B不属于氧化物。他们之间有如图所示的反应关系,图中短线相连的物质间能发生反应。下列说法中,正确的是( )
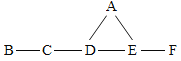
A.相连的物质间发生的反应均属于复分解反应
B.固态C物质可用于人工降雨
C.A与D混合后有气泡产生
D.C与D混合后溶液中始终没有明显现象
【答案】B
【解析】
氧化铁只与盐酸反应,氢氧化钙能与二氧化碳、盐酸和碳酸钠三种物质反应,盐酸能与氧化铁、碳酸钠、氢氧化钠、氢氧化钙四种物质反应,二氧化碳能与氢氧化钙、氢氧化钠两种物质反应,碳酸钠能与盐酸、氢氧化钙两种物质反应,B不是氧化物,B不是氧化铁和二氧化碳,F为氧化铁,则E为盐酸,A为碳酸钠,D为氢氧化钙,C为二氧化碳,B为氢氧化钠。
A、二氧化碳与氢氧化钠的反应是两种化合物生成两种化合物的反应,由于没有相互交换成分,不属于基本反应类型,故A不正确;
B、固态C是干冰,易升华获得低温。可用于人工降雨,故B正确;
C、A是碳酸钠,D是氢氧化钙,两者混合后生成氢氧化钠和碳酸钙沉淀生,故C不正确;
D、C是二氧化碳,D是氢氧化钙,两者混合后生成水和碳酸钙沉淀,故D不正确。故选B。

【题目】金属及其化合物在生产生活中有广泛的应用。
(一)金属的应用和防护
(1)飞机的燃料是航空煤油,它主要是由____炼制的(填“石油”或“煤”)。
(2)铁生锈需要同时接触O2和____,请提出生活中铁制品防锈的一种方法____。
(3)特种钢中的Mn可以由MnO2和Al粉混合在高温下通过置换反应制得,该化学方程式为____。
(4)Mg(OH)2受热分解生成MgO,Mg(OH)2用作阻燃剂,其原理是____(填字母)。
A 分解吸热,降低环境温度 B MgO覆盖燃烧物,隔绝氧气
(二)制备还原性铁粉
实验室利用废铁屑(含少量Fe2O3)为原料制备还原性铁粉的流程如下:
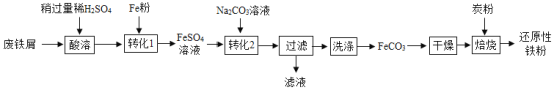
(1)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为____。
(2)检验FeCO3已洗净的方法:取最后一次洗涤后的滤液,先加入一定量稀盐酸,除去CO32-,再滴加____溶液,无明显现象。
(3)“干燥”发生转化:FeCO3 ![]() FeOOH+CO2,该转化的化学方程式为____。
FeOOH+CO2,该转化的化学方程式为____。
(4)“焙烧”前,应将炭粉与“干燥”所得固体均匀混合,目的是____。
(三)测定还原性铁粉的组成
还原性铁粉中含有少量FexCy,小组同学在老师的指导下进行以下实验。
资料:① Fe,FexCy在加热时与O2反应能生成Fe2O3和CO2。
②FexCy不与酸反应。
实验1:取30.48g样品,加入足量稀H2SO4,充分反应后生成1.00gH2。
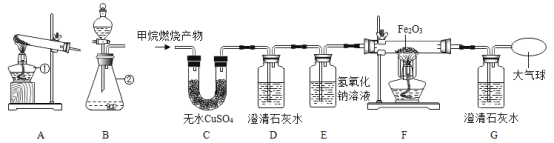
实验2:另取30.48g样品,按下图进行实验。
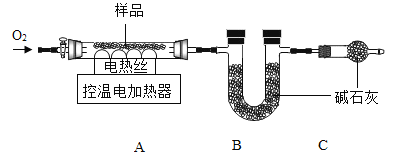
表:装置A和B的质量变化
装置 | A | B |
反应前 | 400.00g | 400.00g |
反应后 | mg | 400.88g |
实验后A中固体全部变为红棕色,装置A、B的质量变化如上表。
(1)装配好装置后,实验前先要____。
(2)装置C的作用是____。
(3)FexCy中,x:y=____。表中m的值是____g。
(实验反思):若用空气(除去CO2)的替代O2进行实验,测得x:y的值偏大,可能的原因是____。
【题目】溶洞都分布在石灰岩组成的山洞中,石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成可溶性的碳酸氢钙:CaCO3+ CO2+ H2O=Ca(HCO3)2。某化学兴趣小组同学们思考:若向碳酸钠溶液中通入一定量的二氧化碳,是否能生成碳酸氢钠(NaHCO3)?于是他们开始实验探究。(不考虑二氧化碳和碳酸作为溶质的情况)
(提出问题)所得溶液中所含溶质成分是什么?
(查阅资料)碳酸氢钠溶液呈碱性。
(提出猜想)猜想一:溶质为Na2CO3;
猜想二:溶质为NaHCO3;
猜想三:溶质为_____。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
①取所得溶液少许于试管中, 向其中滴加过量的CaCl2溶液 | 有白色沉淀生成 | 猜想二___(填“成立”或“不成立”) |
②取实验步骤①中上层清液,滴加适量稀盐酸 | 有气泡冒出 | 猜想一不成立 |
(得出结论)猜想三成立,证明二氧化碳通入碳酸钠溶液生成了碳酸氢钠。写出实验步骤②中发生反应的化学方程式________。
(讨论交流)小明同学认为,向碳酸钠溶液中通入一定量二氧化碳后,再向所得溶液中滴加几滴酚酞溶液,溶液变红就能证明一定有碳酸氢钠生成。小红同学对小明同学的结论产生质疑,其理由是___。
(拓展应用)同学们回忆在实验室用澄清石灰水检验二氧化碳的情景,结合上述知识,如果向一定量的澄清石灰水中不断通入二氧化碳气体,下列哪一个图像能正确反应生成的碳酸钙沉淀与二氧化碳的质量之间的变化关系_____(填字母序号)。
A 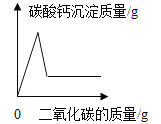 B
B 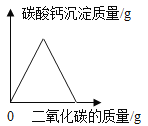 C
C 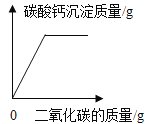
【题目】小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡。为了解其反应过程,他与学习小组的同学进行了如下探究。
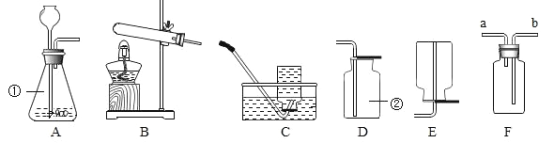
(探究一)小组同学根据所学的化学知识设计并进行了如图所示的实验。
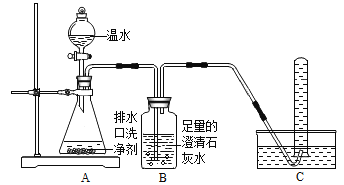
A B C
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺。由此同学们得出结论:生成的两种气体分别是:______(填化学式)。B中有关反应的化学方程式是_____________________________________。
(探究二)
(1)实验过程:
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:

(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设: 根据以上实验现象,X溶液中一定存在的溶质是________;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种。
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3 + CaCl2 ═ CaCO3↓ + 2NaCl。
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同。
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验。请将下列实验方案填写完整。
实验操作 | 主要实验现象 | 结论 |
① |
| 证明溶液中有Na2CO3 |
② |
| 证明溶液中无NaHCO3 |
③ |
| 证明溶液中无NaOH |
(6)实验反思:根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀。于是,同学们猜想:碳酸氢钠与氢氧化钠是否可以发生__________________________(写方程式)这样的反应?于是,同学们进行了新的探究实验。
【题目】某同学在做铝与酸反应的实验中发现了一个怪现象并记录于下表中,为了探究影响反应速率的因素及两者反应差异的原因,该同学做出了以下假设,你认为假设不合理的是
反应时间 | 1 | 2 | 5 | 15 | 20 | |
实验1 | 质量分数 | 极少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
实验2 | 质量分数 | 无明显现象 | 极少量气泡 | |||
A.与盐酸反应开始产生气泡速率慢的原因:铝片表面有氧化膜
B.与盐酸反应产生气泡速率越来越快的原因:反应放热,溶液温度升高
C.两者反应差异的原因:盐酸中有![]() ,稀硫酸中没有
,稀硫酸中没有![]()
D.两者反应差异的原因:![]() 对反应有促进作用,
对反应有促进作用,![]() 对反应有阻得作用
对反应有阻得作用