题目内容
某同学分别用
1g的铁屑、锌粒、镁片与足量的某酸反应以制取氢气.完全反应所需时间与当地的金属价格见表:
你认为实验中一般不选用铁屑、镁片与酸反应制取氢气的主要原因是什么?
答案:略
解析:
解析:
|
一般不选用铁是因为铁与酸反应速度慢.一般不选用镁是因为镁与酸反应的速度快,不便于控制反应,而且镁的价格较高. 本题考查了选择实验药品时,要从反应速度、价格等多方面综合考虑. |

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、乙两个实验方案.
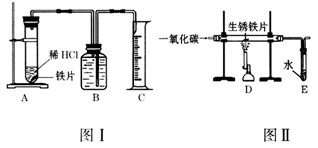
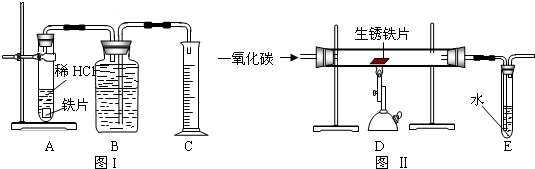
方案甲:称得生锈铁片的质量为m1g,按图Ⅰ所示装置进行实验.完全反应后,测得室温下产生氢气的体积为V1L,查得其密度为
ρ1g/L.方案乙:称得生锈铁片的质量为m2g,先按图Ⅱ所示装置进行实验.当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温.取出铁片,按图Ⅰ所示装置继续进行实验.完全反应后,测得室温下产生氢气的体积为V2L,查得其密度为
ρ2g/L.
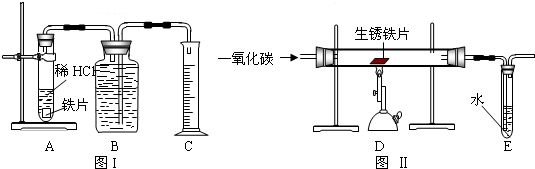
(1)称量是,应将铁片放在托盘天平的 盘(填“左”或“右”);两位同学使用托盘天平,分别称得铁片质量为
2.12g、2.1g,其中不合理的数据是 .
(2)评价交流:上述两个方案中,可行的是 (填“甲”或“乙”);分析不可行方案,其缺陷是 .
(3)设计实验:方案乙中,同学们设计了如下实验报告,请帮助完成.
(4)提出问题:图II所示装置是否有可改进之处?请简要叙述具体改进意见,或在图II中画出简易装置示意图.
(5)结论:生锈铁片中铁元素的质量分数是 (用字母表示)
方案甲:称得生锈铁片的质量为m1g,按图Ⅰ所示装置进行实验.完全反应后,测得室温下产生氢气的体积为V1L,查得其密度为
ρ1g/L.方案乙:称得生锈铁片的质量为m2g,先按图Ⅱ所示装置进行实验.当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温.取出铁片,按图Ⅰ所示装置继续进行实验.完全反应后,测得室温下产生氢气的体积为V2L,查得其密度为
ρ2g/L.

(1)称量是,应将铁片放在托盘天平的
2.12g、2.1g,其中不合理的数据是
(2)评价交流:上述两个方案中,可行的是
(3)设计实验:方案乙中,同学们设计了如下实验报告,请帮助完成.
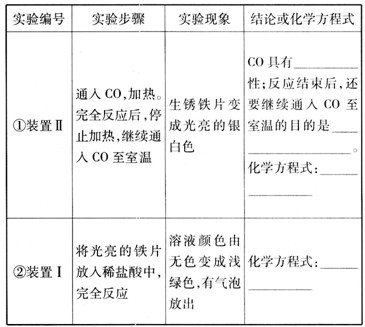
| 实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
① 装置Ⅱ |
通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 |
CO具有 化学方程式: |
| ② 装置Ⅰ |
将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式: |
(5)结论:生锈铁片中铁元素的质量分数是
为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、乙两个实验方案.
方案甲:称得生锈铁片的质量为m1g,按图Ⅰ所示装置进行实验.完全反应后,测得室温下产生氢气的体积为V1L,查得其密度为
ρ1g/L.方案乙:称得生锈铁片的质量为m2g,先按图Ⅱ所示装置进行实验.当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温.取出铁片,按图Ⅰ所示装置继续进行实验.完全反应后,测得室温下产生氢气的体积为V2L,查得其密度为
ρ2g/L.
(1)称量是,应将铁片放在托盘天平的______盘(填“左”或“右”);两位同学使用托盘天平,分别称得铁片质量为
2.12g、2.1g,其中不合理的数据是______.
(2)评价交流:上述两个方案中,可行的是______(填“甲”或“乙”);分析不可行方案,其缺陷是______.
(3)设计实验:方案乙中,同学们设计了如下实验报告,请帮助完成.
| 实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
① 装置Ⅱ | 通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | CO具有______性;反应结束后,还要继续通CO至室温的目的是______ 化学方程式:______ |
| ② 装置Ⅰ | 将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式:______ |
(5)结论:生锈铁片中铁元素的质量分数是______(用字母表示)