题目内容
【题目】已知AgNO3与NaCl反应可生成AgCl,每次新生成的AgCl有10%见光分解成单质银和氯气,氯气又可在水中发生反应:3Cl2+3H2O→HClO3+5HCl,而生成的HCl与剩余AgNO3作用生成AgCl,这样循环往复直到最终。现有含1.1mol NaCl的溶液,加入足量的AgNO3溶液,则最终能生成难溶物(Ag和AgCl)的质量为________克。
【答案】167.94g
【解析】
解:NaCl的溶液,加入足量的AgNO3溶液, 发了三个反应:①Ag++Cl-=AgCl↓;②2AgCl![]() 2Ag+Cl2↑;③3Cl2+3H2O=ClO3-+5Cl-+6H+;①+②+③得: 60Ag++55Cl-+3H2O=54AgCl↓+6Ag↓+
2Ag+Cl2↑;③3Cl2+3H2O=ClO3-+5Cl-+6H+;①+②+③得: 60Ag++55Cl-+3H2O=54AgCl↓+6Ag↓+![]() +6H+ ;解:设生成银的物质量为x,氯化银物质量为y。
+6H+ ;解:设生成银的物质量为x,氯化银物质量为y。
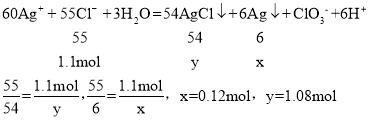
则最终能生成(Ag和AgCl)的质量为:108g/mol×0.12mol+143.5g/mol×1.08mol=167.94g

【题目】碳酸钠、碳酸氢钠是生活中两种常见的重要的盐。
(1)碳酸钠(俗称纯碱、苏打)与碳酸氢钠(俗称_____),均为________色固体,水溶液均呈_______性,向它们的水溶液中分别滴入无色酚酞试液,酚酞试液均变红色。
(2)碳酸钠、碳酸氢钠均可与稀盐酸反应,其中碳酸钠与稀盐酸反应的化学方程式为_____。但是,碳酸钠、碳酸氢钠与稀盐酸反应产生二氧化碳的速率是否相同?校兴趣小组同学针对于此,展开探究:
(方案设计)
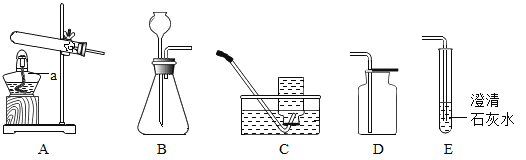
①甲设计的实验如图1所示,实验时,同时全部推出足量稀盐酸后,观察到图2所示现象。于是他得出______和稀盐酸反应产生二氧化碳较快的结论。
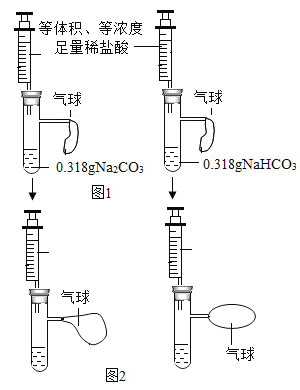
②乙同学通过计算可知:0.318 g碳酸氢钠约产生0.167 g二氧化碳,而0.318 g碳酸钠产生二氧化碳的质量为______g,等质量的碳酸钠与碳酸氢钠与足量的稀盐酸作用,碳酸氢钠产生二氧化碳的质量更多,显然甲同学的设计不妥,应取含碳元素质量相同的碳酸钠和碳酸氢钠进行实验。若碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为_______g。
③小组同学在老师指导下设计了图3所示实验。连通管除消除稀盐酸滴入占有体积引起的误差,还有______的作用。
分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液)以及相同体积、相同浓度的足量稀盐酸进行实验。实验时,广口瓶内压强随时间变化如图4所示,溶液颜色变化记录如表1。
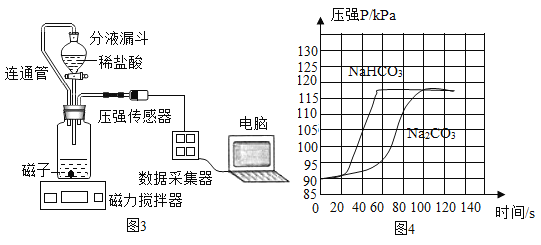
表1:
滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
碳酸氢钠溶液 | 浅红色 | 淺红色→无色 |
(实验结论)分析图4所示的实验数据可得到:相同条件下,碳酸氢钠与稀盐酸反应产生二氧化碳速率更快,你判断的理由是_______。
(实验反思)小组同学分析表1实验现象和图4数据,得出碳酸钠能与稀盐酸反应产生二氧化碳,反应是分步进行的。第一步发生的化学反应方程式是:_______,第二步发生的反应是:NaHCO3+HCl=NaCl+H2O+CO2↑。