题目内容
【题目】钛(Ti)被称为“21世纪的金属”。下图是利用钛白粉(TiO2)生产海绵钛(Ti)的工艺流程:
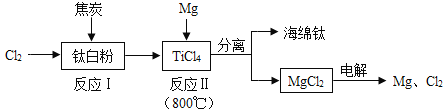
①反应Ⅰ的化学方程式为:2Cl2+TiO2+2C=TiCl4+2X,则X的化学式为_____________。
②反应Ⅱ的化学方程式是_______________________________。
③该工艺流程中,可以循环使用的物质有镁和___________。
【答案】 CO。 2Mg+TiCl4![]() 2MgCl2+Ti; 氯气。
2MgCl2+Ti; 氯气。
【解析】(1)根据质量守恒定律,反应物中有4个氯原子,1个钛原子,2个氧原子,2个碳原子,生成物中已经有1个钛原子,4个氯原子,则2X中含有2个碳原子和2个氧原子,故X 中含有1个碳原子和1个氧原子,故X是CO;
(2)反应Ⅱ是镁与TiCl4反应生成氯化镁和钛,反应方程式为2Mg+TiCl4![]() 2MgCl2+Ti;
2MgCl2+Ti;
(3)由图可知,该过程中可以循环利用的物质有镁和氯气;

 应用题作业本系列答案
应用题作业本系列答案【题目】利用下图装置探究物质的性质(部分固定装置略)。

①仪器 a 的名称___________; 装置 A 中反应的化学方程式___________。
②装置 C 的作用___________;装置 D 中反应的化学方程式为___________ 。
③ 装置 E 中固体由黑色变成亮红色,反应化学方程式为___________;
④ 装置 F 是安全瓶,其作用是___________。
⑤把装置 A 中换成酒精灯,可用于氯酸钾与二氧化锰混合制取氧气。 试管中固体的质量随反应时间变化的数据见下表。
反应时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 26.0 | 20.2 | 16.4 | 16.4 |
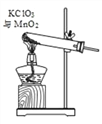
Ⅰ.共制得氧气的质量是_________g;
Ⅱ.参加反应的氯酸钾的物质的量是_________mol(通过化学方程式列式计算)。

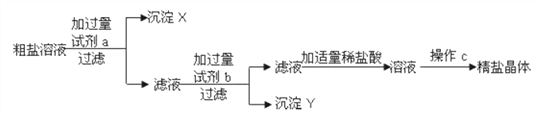
【题目】氯化钠、碳酸钠不同温度下的溶解度如下表所示,请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | 碳酸钠 | 7.0 | 12.5 | 21.5 | 39.7 | 49.0 |
氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | |
(1)20℃时,30g碳酸钠和30g氯化钠的固体混合物加入到100g水中,充分搅拌后_____(填“是”或“否”)有固体剩余。
(2)生活在盐湖附近的人们“夏天晒盐(氯化钠)”、“冬天捞碱(碳酸钠)”,其冬天捞碱依据的原理是___________(填“蒸发结晶”或“降温结晶”)。
(3)将300g碳酸钠溶液和150g石灰水溶液混合后,恰好完全反应,过滤,得到白色沉淀50g,则所得的滤液中溶质的质量分数多少_____________?。