题目内容
【题目】利用下图装置探究物质的性质(部分固定装置略)。
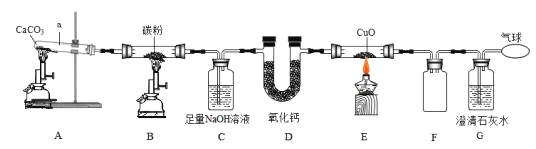
①仪器 a 的名称___________; 装置 A 中反应的化学方程式___________。
②装置 C 的作用___________;装置 D 中反应的化学方程式为___________ 。
③ 装置 E 中固体由黑色变成亮红色,反应化学方程式为___________;
④ 装置 F 是安全瓶,其作用是___________。
⑤把装置 A 中换成酒精灯,可用于氯酸钾与二氧化锰混合制取氧气。 试管中固体的质量随反应时间变化的数据见下表。
反应时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 26.0 | 20.2 | 16.4 | 16.4 |
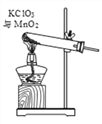
Ⅰ.共制得氧气的质量是_________g;
Ⅱ.参加反应的氯酸钾的物质的量是_________mol(通过化学方程式列式计算)。

【答案】 试管 CaCO3![]() CaO+CO2↑ 吸收二氧化碳 CaO+H2O=Ca﹙OH﹚2 CuO+CO
CaO+CO2↑ 吸收二氧化碳 CaO+H2O=Ca﹙OH﹚2 CuO+CO![]() Cu+CO2 保护 9.6 0.2
Cu+CO2 保护 9.6 0.2
【解析】探究物质的性质。①仪器 a 的名称是试管;装置 A 中反应的化学方程式是CaCO3高温CaO+CO2↑。②装置 C 的作用吸收二氧化碳,氢氧化钠溶液与二氧化碳反应生成碳酸钠;装置 D 中反应的化学方程式为CaO++H2O=Ca﹙OH﹚2。③ 装置 E 中固体由黑色变成亮红色,反应化学方程式为CuO+CO △Cu+CO2。④ 装置 F 是安全瓶,其作用是保护,把装置中的空气排入,防止意外事故发生。⑤把装置 A 中换成酒精灯,可用于氯酸钾与二氧化锰混合制取氧气。Ⅰ.根据质量守恒定律知,共制得氧气的质量是26.0g-16.4g=9.6g;Ⅱ. 生成氧气物质的量是![]() =0.3 mol
=0.3 mol
解∶设参加反应的氯酸钾的物质的量是x_mol
2KClO3 MnO2 2KCl+3O2↑
2 3
X 0.3 mol
![]() =
=![]() ,x=0.2mol。
,x=0.2mol。
所以参加反应的氯酸钾的物质的量是0.2mol。
点睛∶化学方程式的书写应遵循⑴以客观事实为依据⑵遵循质量守恒定律。碳酸钙煅烧可以分解生成氧化钙,氧化钙与水反应生成氢氧化钙。

 步步高达标卷系列答案
步步高达标卷系列答案