题目内容
【题目】新型冠状病毒肺炎威胁着人们的身体健康。高温、紫外线、强酸强碱、强氧化剂等都能使 新冠病毒的蛋白质外壳变性,起到消杀病毒的作用。为消杀新型冠状病毒,84 消毒液、过氧乙酸、75% 的消毒酒精等医用消毒剂走进千家万户。
资料一:84 消毒液[有效成分为次氯酸钠(NaClO)]和 ClO2,是常用的含氯消毒剂。
资料二:酒精易挥发、易燃,常用作酒精灯和内燃机的燃料。使用 75%的酒精消毒时一定要注意防火!
资料三:过氧乙酸(C2H4O3)是一种高效消毒剂。根据资料回答下列问题:
(1)NaClO 属于_____(填字母序号)。
A 混合物 B 化合物 C 氧化物
(2)ClO2 的物质名称读成_________。
(3)使用 84 消毒液时,往往需要稀释成不同的浓度。现欲将 84 消毒液按 1:200 的体积比稀释,配 制成教室消毒液。已知 84 消毒液的瓶盖盛满消毒液约 10 mL,1 个空矿泉水瓶子盛满水约 250 mL。则 1 瓶盖 84 消毒液需要加____ 瓶水可以稀释成约 1:200 的消毒液。
(4)从资料二中,可归纳出酒精的物理性质是_____,酒精的用途是_____
(5)实验中,不小心将酒精灯碰倒在桌上燃烧起来,简单合理的灭火措施是_________。
(6)过氧乙酸(C2H4O3)中氢、氧元素的质量比为____,碳元素的质量分数为____(精确到 0.1%)。
【答案】B 二氧化氯 8 易挥发 作燃料和消毒剂 用湿毛巾盖灭 1:12 31.6%
【解析】
(1)NaClO 是由钠、氯和氧三种元素组成的纯净物,属于化合物,故选B。
(2)ClO2 的物质名称读成二氧化氯。
(3)设需要水的体积为x。则有
1:200= 10 mL:x ,解得x=2000 mL。
![]() 。
。
(4)根据资料二,可知酒精的物理性质是易挥发,酒精的用途是作燃料和消毒剂。
(5)实验中,不小心将酒精灯碰倒在桌上燃烧起来,简单合理的灭火措施是用湿毛巾盖灭,既可降温,又能隔绝氧气。
(6)过氧乙酸(C2H4O3)中氢、氧元素的质量比为![]() ,碳元素的质量分数为
,碳元素的质量分数为![]() 。
。

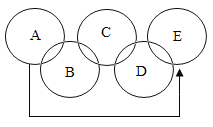
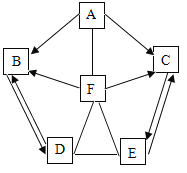
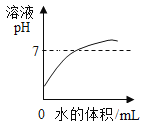
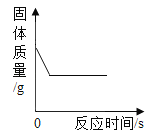
【题目】下图所示的四个图像分别与实验操作对应关系正确的是
图像对应 的变化关 系 |
|
|
|
|
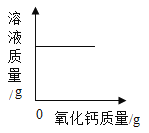
实验操作 | A 一定质量某盐酸中加水稀释 | B 一定质量二氧化锰固体中加入一定质量的过氧化氢溶液 | C 温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙 | D 一定质量硫酸和硫酸铜混合溶液中加入氢氧化钠溶液 |
A.AB.BC.CD.D