题目内容
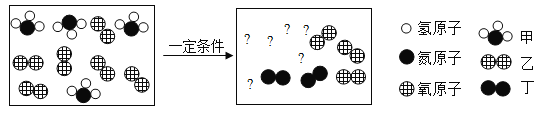
【题目】某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及的反应均为初中化学常见的反应,且各步均恰好完全反应)。
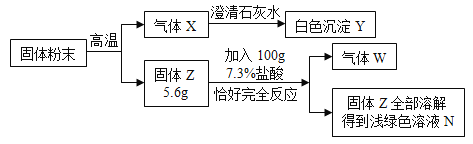
下列说法中正确的是
A.溶液N中只含一种溶质
B.原固体粉末中一定含有碳酸钙
C.白色沉淀Y是碳酸钙,气体W是氢气
D.原固体粉末中一定没有氧化铜,一定含有碳酸钙
【答案】C
【解析】
碳酸钙在高温的条件下生成氧化钙和二氧化碳,木炭和氧化铜在高温的条件下生成铜和二氧化碳,木炭和氧化铁高温生成铁和二氧化碳,铜不会与酸反应,铁和盐酸反应生成浅绿色的氯化亚铁和氢气,氧化钙也会与盐酸反应生成氯化钙。固体粉末高温的条件下生成气体X,X能使澄清的石灰水变浑浊,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,说明X是二氧化碳,Y是碳酸钙;固体Z5.6g加入100g7.3%的盐酸恰好完全反应,生成气体W,固体Z全部溶解得到浅绿色溶液N,因此Z中有铁,W是氢气,浅绿色溶液N中有氯化亚铁溶液;因此原固体粉末中一定有氧化铁和木炭粉,一定没有氧化铜,碳酸钙可能存在也可能不存在;因此溶液N中一定含有氯化亚铁,可能含有氯化钙。
A、溶液N中一定含有氯化亚铁,可能含有氯化钙。故A错误;
B、原固体粉末不一定含有碳酸钙,故B错误;
C、白色沉淀Y是碳酸钙,气体W是氢气,故C正确;
D、原固体粉末中一定没有氧化铜,可能含有碳酸钙,故D错误。故选C。

【题目】(1)用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液pH变化曲线如图所示:
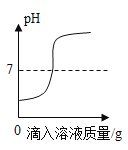
①该反应的化学方程式是________________;
②该实验操作是将__________(写溶质的化学式)溶液逐滴加入到另一种溶液中。
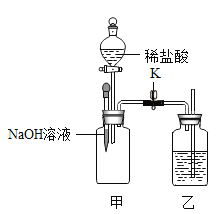
(2)若用稀硫酸代替(1)中的稀盐酸,将稀硫酸逐滴加入至盛有氢氧化钠溶液的烧杯中,当滴加到一定量并充分反应时,请对烧杯中溶质成分进行探究。
(提出问题)此时烧杯中的溶质成分是什么?
(猜想与假设)Ⅰ:Na2SO4;Ⅱ:_____________;Ⅲ:Na2SO4和NaOH。
(实验与探究)
实验步骤 | 实验现象 | 实验结论 |
取少量上述烧杯中的溶液于试管中,滴加_______溶液 | _______________ | 猜想Ⅱ正确 |
取少量上述烧杯中的溶液于试管中,滴加_______溶液 | ______________ | 猜想Ⅲ正确 |