题目内容
【题目】实验室要配制50g 10%的氯化钠溶液,其操作示意图如图所示.
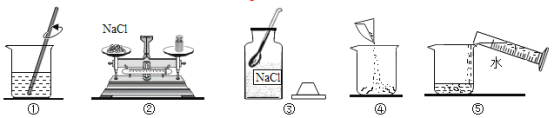
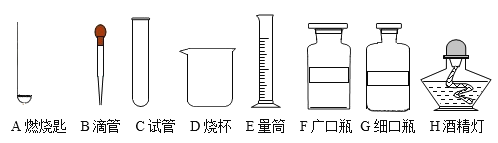
(1)称量氯化钠所用的仪器是__(填名称);
(2)①中玻璃棒的作用是__;
(3)该实验的正确操作顺序为_______(填数字序号);
(4)如果前面配制的溶液中溶质的质量分数小于10%,其原因可能有__;
A.量筒读数时,俯视 B.固体倒入烧杯时洒落
C.配制时烧杯不干燥 D.装瓶时有液体溅出
(5)若将配制好的50g 10%的氯化钠溶液,稀释为质量分数为5%的氯化钠溶液,需加一定量的水时所用到的仪器是__________(填名称);加水的质量为__g.
【答案】天平 加快溶解 ③②④⑤① B、C 量筒、胶头滴管 50
【解析】
解:(1)称量氯化钠所用的仪器是托盘天平;
(2)①中玻璃棒的作用是搅拌加速食盐的溶解;
(3)配制溶液的步骤是:计算、称量、溶解、装瓶存放,因此实验的正确操作顺序为:③②④⑤①;
(4)A、量取水时俯视读数,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大;
B、固体倒入烧杯时洒落,造成溶质少了,将导致溶质质量分数偏小;
C、配制时烧杯不干燥,造成溶剂质量偏大,将导致溶质质量分数偏小;
D、装瓶时有液体溅出,溶质质量分数无影响;
(5)设稀释后所得5%的氯化钠溶液质量为x,则50g×10%=5%×x,解得x=100g.则需加水的质量为:100g-50g=50g;量取一定体积的水需要量筒和胶头滴管。

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目