题目内容
【题目】兴趣小组的同学通过查阅资料获知:将新制的溶质质量分数为 5%的过氧化氢溶液,加热到 80℃时,才有较多氧气产生;而相同质量、溶质质量分数为 5%的过氧化氢溶液加入催化剂,常温下就会立即产生氧气,反应速度快,所需时间短。
下面是兴趣小组同学进行实验的装置图及画出的曲线图,请据图回答下列问题:
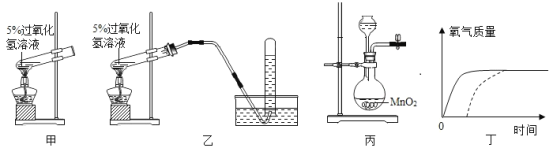
(1)请写出上图装置中任意两种仪器的名称: _________、_____。
(2)小晨按图甲装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃。为此,他利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星木条未复燃的原因是_____。乙装置中产生氧气的化学方程式是_______。
(3)小柯利用催化剂使过氧化氢溶液分解制取氧气,图丙是他设计的气体发生装置,请你指出存在的一处错误_____________。
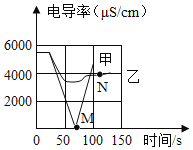
(4)取相同质量、溶质质量分数均为 5%的过氧化氢溶液,采用加热或利用催化剂分解过氧化氢的方法制取氧气得到如图丁所示的曲线,请写出实线和虚线所采用的制取氧气的方法(假定两种方法过氧化氢均完全分解)。
实线:_________,虚线____________。
【答案】试管 铁架台 加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少 2H2O2![]() 2H2O+O2
2H2O+O2![]() 长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出 加入二氧化锰的反应 未加二氧化锰的反应
长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出 加入二氧化锰的反应 未加二氧化锰的反应
【解析】
(1)上图装置中包含试管、铁架台、酒精灯、水槽等,任意两种即可;
(2)图甲实验中带火星木条未复燃的原因是:加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;乙装置中发生的反应为双氧水在二氧化锰的催化下反应生成氧气和水,方程式为:2H2O2![]() 2H2O+O2
2H2O+O2![]() ;
;
(3)在图丙的气体发生装置中,错误是:长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出.
(4)由于过氧化氢在二氧化锰催化作用下能很快分解放出氧气,实线表示加入二氧化锰的反应,虚线表示未加二氧化锰的反应。

【题目】某小组同学在实验室研究铝与氯化铜溶液的反应。
实验操作 | 实验现象 |
| ①红色物质附着于铝片表面 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色沉淀和白色沉淀 |
(1)打磨铝片的目的是__________。
(2)现象①和现象③中的红色物质均为Cu,生成该物质的化学方程式为______________。
(3)经检验,现象②中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性,经pH计检验,pH_____7,证实了甲的猜想。
(4)探究白色沉淀的化学成分。
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
CuCl中铜元素的化合价是________。
【查阅资料】
①CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl-。
②Cu(NH3)2+在空气中易被氧化变为蓝色;Cl-可与硝酸银溶液反应,产生白色沉淀。
【进行实验】
①取烧杯底部的白色沉淀,充分洗涤;
②向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
③取其中一份无色溶液……
④将另一份无色溶液放置于空气中……
以上步骤③的实验方案是________;步骤④的现象是________。
【得出结论】通过实验可以确定,该白色固体是CuCl。
【反思与评价】Al和CuCl2溶液反应为什么会出现CuCl呢?
丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl。
丙同学为了验证猜想,取Cu粉与15% CuCl2溶液混合,无白色沉淀产生。
(5)丙通过分析Al与CuCl2溶液反应的实验现象,改进了实验,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是________。
(6)丁同学认为丙同学的实验还不够严谨,还应考虑________对Cu与CuCl2溶液反应的影响。
【题目】甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
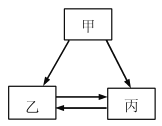
选项 | 甲 | 乙 | 丙 |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Ca(OH)2 | CaCl2 | CaCO3 |
D | NaOH | NaCl | NaNO3 |
A. A B. B C. C D. D