题目内容
【题目】在下面关系图中,A、B、C、D是初中化学中常见的单质,甲、乙分别是酒精燃烧时一定会产生的两种物质,丁是常用建筑材料的主要成分,G为无色有刺激性气味的气体,能使紫色石蕊变蓝,J是赤铁矿的主要成分。

(1)写出化学式:甲是_____,丁是_____,G是_____;
(2)写出A与B反应的化学方程式:_____;
(3)写出E→F的化学方程式:_____。
【答案】H2O CaCO3 NH3 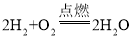
![]()
【解析】
丁是常用建筑材料的主要成分,所以丁是碳酸钙;G为无色有刺激性气味的气体,能使紫色石蕊变蓝,所以G是氨气;J是赤铁矿的主要成分,所以J是氧化铁;甲、乙分别是酒精燃烧时一定会产生的两种物质,甲可能是水,乙可能是二氧化碳;丙是碳酸;碳酸和F反应生成碳酸钙,则F可能是氢氧化钙;E和水生成氢氧化钙,E是氧化钙;碳酸钙在高温的条件下生成氧化钙和二氧化硫,所以乙是二氧化碳;A、B、C都是单质,A和B点燃生成水,B和C点燃生成二氧化碳,所以A是氢气;B是氧气;C是碳;二氧化碳和碳反应生成H,H是一氧化碳;一氧化碳和氧化铁反应生成铁和二氧化碳,D是单质,D是铁,把以上各物质代入框图进行验证,符合要求。
(1)根据分析可知,甲是水,化学式是H2O,丁是碳酸钙,化学式是CaCO3,G是氨气,化学式是 NH3;
(2)氢气和氧气在点燃的条件下生成水,化学方程式为: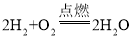 ;
;
(3)氧化钙和水反应生成氢氧化钙,化学方程式为:![]() 。
。

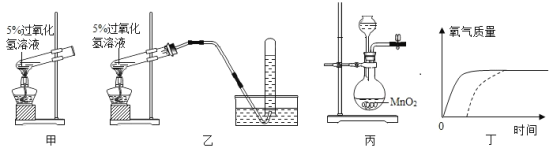
【题目】实验室有两瓶保管不当的试剂(如图1),左瓶残缺的标签中只剩下“Na”和“10%”字样,已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种;右瓶是敞口放置的30%的NaOH溶液。同学们很感兴趣,决定对其成分进行探究:

Ⅰ.甲同学对左瓶标签残缺的溶液展开研究:
(提出问题)这瓶试剂可能是什么溶液呢?
(交流讨论)根据受损标签的情况判断,这瓶试剂不可能是_____。(填字母)
A 酸 B 碱 C 盐
(查阅资料)
①Na2CO3和NaHCO3溶液都呈碱性。
②测定室温(20℃)时,四种物质的溶解度的数据如下
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
(得出结论)根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是_____。
(设计实验并继续探究)
(1)用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是_____。
(2)为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
操作步骤 | 实验现象 | 结论及化学方程式 |
取样于试管中,滴加足量的 _____ | 有气泡产生 | 该溶液是_____ 相关的化学方程式_____ |
Ⅱ.乙同学对右瓶敞口放置的溶液展开研究:
(1)乙同学根据氢氧化钠固体及溶液在空气中很容易发生变质生成碳酸钠,对其变质情况进行了如下探究。
(猜想与假设)该氢氧化钠溶液已部分变质。氢氧化钠溶液变质的反应方程式是_____。
(实验与结论)
实验步骤 | 实验现象 | 实验结论 |
a.取少量该溶液于一支试管中,加入足量_____ | 有白色沉淀产生 | 该氢氧化钠溶液已变质 |
b.将步骤a所得的液体静置,取上层清液于另一支试管中,滴加_____ /td> | _____ | 该氢氧化钠溶液已部分变质 |
实验步骤a中加入的试剂必须足量的原因是:
(拓展探究)乙同学又尝试通过实验除去该氢氧化钠溶液中含有的碳酸钠,方案如下:
向该溶液中加入适量的_____溶液,充分反应后,经_____操作,即可除去该氢氧化钠溶液中含有的杂质。
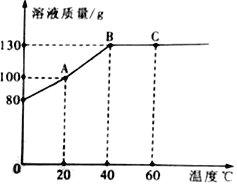
Ⅲ.丙同学查阅资料得知:碳酸钠与稀盐酸反应分两步进行:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,他取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸。实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图2所示。下列说法正确的是_____。
A N点的溶液表示氢氧化钠被恰好完全反应
B PQ段(不含P点)溶液的pH<7
C NP段表示产生气体的过程,a的值为210.2
D 该固体样品中氢氧化钠的质量为8.0g。