��Ŀ����
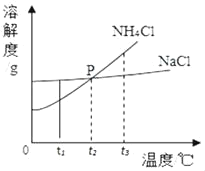
����Ŀ���ס��ҡ����������ʵ��ܽ��������ͼ��ʾ������˵��������ǣ�������

A. ���������ʵIJ�������Һ��Ϊ������Һ���ɲ�ȡ�����¶ȵķ���
B. t2��ʱ��30g�����ʼ���50gˮ�У���ֽ����������Һ�����ʵ���������Ϊ37.5%
C. ����ͬ�����ļס��ҡ����������ʵı�����Һ��t2�潵�µ�t1�棬�������������Ǽ�
D. t1��ʱ���ס��ҡ����������ʵ��ܽ���ɴ�С��˳���ǣ��ң��ף���
���𰸡�B
��������
A�������ʵ��ܽ�����¶ȵ����߶���С�����������ʵIJ�������Һ��Ϊ������Һ���ɲ�ȡ�����¶ȵķ�������A��ȷ��
B��t2��ʱ�������ʵ��ܽ����50g�������ܽ�ȸ����֪��t2��ʱ��100gˮ������ܽ�30g�ļף�����30g�����ʼ���50gˮ�У���ֽ����������Һ�����ʵ���������Ϊ![]() ����B����
����B����
C�������ʵ��ܽ�����¶ȱ仯Ӱ��ϴ����Խ���ͬ�����ļס��ҡ����������ʵı�����Һ��t2�潵�µ�t1�棬�������������Ǽף���C��ȷ��
D��ͨ�������ܽ�����߿�֪��t1��ʱ���ס��ҡ����������ʵ��ܽ���ɴ�С��˳���ǣ��ң��ף�������D��ȷ����ѡB��

����Ŀ���γDZ��ٻƺ�����ˮ�к���NaCl��CaCl2��
��1�����з������ܵ�����ˮ����_____������ĸ����
A�ֽⷨ B������ C����
��2���Ӻ�ˮ�л�ȡ���Σ���ѡ��_____�����������ᾧ���������½ᾧ������Ϊ�˳�ȥ������Һ�е�Ca2+��Mg2+��SO42�����ɰ�������ʵ�鲽����У��ټӹ���BaC12��Һ���ڼӹ���NaOH��Һ���ۼӹ���Na2CO3��Һ���ܲ���X���ݼ����������ᡣ���в���ۼӹ���Na2CO3��Һ��Ŀ����_____������ܲ���X��������_____��
��3����ˮ��þ���̣�
![]()
д��b���跢����Ӧ�Ļ�ѧ����ʽ_____����ȡ�Ȼ�þ����a��b����ת����Ŀ����_____������a�������ɵ�������þ��Ҫϴ�ӣ�����������þ�Ƿ�ϴ���ķ����ǣ�ȡ�������һ��ϴ��Һ���Թ��У��μ�����ϡ�����_____��Һ�����ް�ɫ�������ɣ�˵����ϴ����
��4����Ϊ�Ȼ����ڲ�ͬ�¶�ʱ���ܽ�ȡ���ϱ������ݻش�
�¶�/�� | 30 | 50 | 70 | 100 |
�ܽ��/g | 36.3 | 37.0 | 37.8 | 39.8 |
����100g��������Ϊ10%���Ȼ�����Һ������50����Ȼ��Ʊ�����Һ����Ϊ_____g�������ȷ��1g����
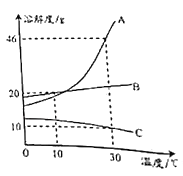
��5��CaCl2Ӧ�ù㷺����ʯ��ʯ��������Ҫ��Fe2O3��MgSO4��Ϊԭ������CaCl2��������ͼ��
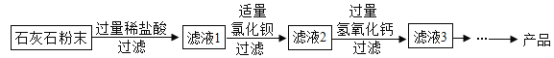
��Һ1�е�������HCl��FeCl3��MgSO4��_____���ѧʽ����
����Һ2�м���Ca��OH��2���Գ�ȥHCl��MgCl2��_____���ѧʽ����
����Ŀ������ʯ��ʯ����Ҫ�ɷ� CaCO3��������ʯ�ң�CaO���Ͷ�����̼��Ϊ�˲ⶨijʯ��ʯ��̼��ƣ�CaCO3���ĺ������ֳ�ȡ 24.0g ʯ��ʯ��Ʒ�������Ĵθ������ա���ȴ������ʣ���������� �����ʲ��μӷ�Ӧ������¼ʵ���������£�
���� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
ʣ��������� | 21.6g | 19.2g | 15.2g | 15.2g |
�Լ��㣺
��1����ȫ��Ӧ�����ɶ�����̼������Ϊ_____��
��2�����ʯ��ʯ��Ʒ��̼��Ƶ�����_____��