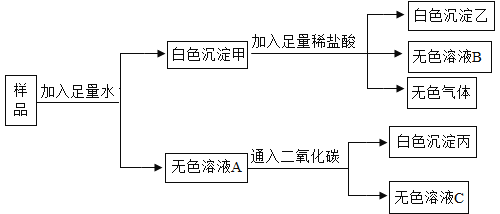
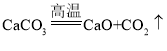题目内容
【题目】如图所示,试管中盛有一段镁条,向试管中加入过量稀盐酸,观察到 U 形管中 a 处液面下降,b 处液面上升。回答下列问题:
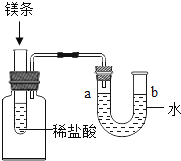
(1)镁条与稀盐酸反应的化学方程式为________。
(2)U 形管中液面发生变化的原因是________。
(3)完全反应后,试管中的溶质有________。
(4)将试管中的物质换成水和另一种固体,也可以让 U 型管内液面发生同样的变化, 则“另一种固体”是____
【答案】Mg+2HCl=MgCl2+H2↑ 反应放热,瓶内的气压增大 氯化镁和氯化氢 生石灰
【解析】
(1)镁条和稀盐酸反应生成氯化镁和氢气,反应的化学方程式是Mg+2HCl=MgCl2+H2↑;故填:Mg+2HCl=MgCl2+H2↑;
(2)镁条和稀盐酸反应生成氯化镁和氢气,因为此反应是放热反应,广口瓶中的气压增大,所以还可看到a液面降低b液面升高;故填:a液面降低b液面升高;
(3)镁条与稀盐酸反应生成氯化镁和氢气,因为盐酸过量,完全反应后,试管中的溶质有氯化镁和氯化氢,故填:氯化镁和氯化氢;
(4)生石灰与水反应放出大量的热,广口瓶中的气压增大,也可看到a液面降低b液面升高;故填:生石灰。

练习册系列答案
相关题目