题目内容
【题目】宏微相结合是认识物质结构的有效方法之一。
(1)已知:X、Y、X、W 四种粒子的核电荷数及核外各电子排布情况如下表:
粒子 | X | Y | Z | W | |
对应元素名称 | 氧 | 镁 | 铝 | 氯 | |
核电荷数 | 8 | 12 | 13 | 17 | |
电子层 | 第一层 | 2 | 2 | 2 | 2 |
第二层 | a | 8 | 8 | 8 | |
第三层 | 3 | 8 | |||
请回答下列问题:
①若 X 表示原子,a= ___。单质X2与单质 Z 的反应中,X 原子____(填“得到”或“失 去”)电子。
②Y、W 形成的化合物化学式为____(用元素符号表示)。
(2)甲和乙可以合成清洁燃料丙,微观过程如图所示。回答下列问题:
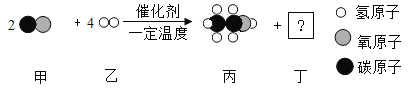
①丁物质的1个分子中由____________个原子构成。
②丙中C、H、O的质量比为____________。
③写出丙物质作燃料的化学方程式____________。
【答案】6 得到 MgCl2 3 12﹕3﹕8 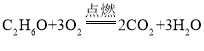
【解析】
(1)①若 X 表示原子,原子中质子数=核外电子数,所以a=82=6,故填6;
由图可知,X原子为氧原子,其最外层电子数为6,在化学反应中容易得到电子,故填得到。②由图可知,Y为镁元素,W为氯元素,镁元素的化合价为+2价,氯元素的化合价为-1价,根据化合物中各元素的化合价的代数和为零,Y、W元素组成的化合物的化学式为MgCl2,故填MgCl2。
(2)①由图可知,反应前甲中的原子的数目是4,乙中的原子的数目是,8,生成物丙中的原子的数目是9,根据质量守恒定律的原因可知,丁中的原子的数目=4+89=3,故填3;
②由图可知,1个丙分子中含有2个碳原子、6个氢原子和1个氧原子,所以丙中C、H、O的质量比=(12×2):(1×6):16=12:3:8,故填12:3:8;
③由图可知,1个丙分子中含有2个碳原子、6个氢原子和1个氧原子,则丙为乙醇,乙醇与氧气在点燃的条件下反应生成二氧化碳和水,故反应的化学方程式写为:C2H6O+3O2![]() 2CO2+3H2O。
2CO2+3H2O。

 全能练考卷系列答案
全能练考卷系列答案