题目内容
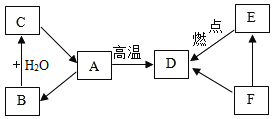
【题目】氨气易溶于水,易与浓硫酸反应,不与碱石灰(干燥剂)反应.氨气还具有还原性,在加热的条件下能还原氧化铜:2NH3+3CuO![]() N2+3Cu+3H2O,某化学兴趣小组同学设计下图所示实验来验证氨气的组成(图中夹持、固定装置部分均略去).已知整套装置气密性良好,且实验中所用试剂均足量,B、D、E中所装药品能完全吸收相关物质.实验前装置 C、D 的质量分别为 mC1、mD1.
N2+3Cu+3H2O,某化学兴趣小组同学设计下图所示实验来验证氨气的组成(图中夹持、固定装置部分均略去).已知整套装置气密性良好,且实验中所用试剂均足量,B、D、E中所装药品能完全吸收相关物质.实验前装置 C、D 的质量分别为 mC1、mD1.

实验步骤:
Ⅰ.连接装置A、B、C、D、E,打开分液漏斗旋塞注入足量浓氨水后关闭旋塞.通入氨气一段时间后,接着连接装置F.
Ⅱ.点燃酒精灯加热,待黑色固体变为红色后,停止加热.
Ⅲ.继续通氨气至玻璃管冷却.
Ⅳ.记录量气管读数为V mL.
V.称量装置 C、D 的质量分别为 mC2、mD2.
请回答下列问题:
(1)装置A中NaOH固体所起的作用,是利用了该物质的____性质.
(2)若 mC1﹣mC2=(mD2﹣mD1)×____,则可证明氨气的组成中不含氧元素.
(3)步骤Ⅲ通入氨气的目的之一是____.
(4)如果略去装置B,导致的后果是____.
①装置C中会发生新的化学反应
②会得出“氨气的组成中含有氧元素”的结论
③使测得的氨气组成中N、H元素质量比偏大
(5)为减小误差,在读取量气管读数前必须进行的操作是____.
(6)步骤Ⅱ中氧化铜是否完全反应,对实验结果____(填“有”、“没有”或“不确定有没有”)影响.
【答案】遇水溶解放热 ![]() 排出装置内生成物,减小误差 ② 调节水准管,使量气管与水准管液面相平 没有
排出装置内生成物,减小误差 ② 调节水准管,使量气管与水准管液面相平 没有
【解析】
(1)氢氧化钠固体溶于水放出大量的热,所以装置A中NaOH固体所起的作用,是利用了该物质遇水溶解放热的性质;
(2)(mD2-mD1)是反应生成水的质量,水中氧元素的质量分数是![]() ,所以mC1-mC2=(mD2-mD1)×
,所以mC1-mC2=(mD2-mD1)×![]() ,可证明氨气的组成中不含氧元素;
,可证明氨气的组成中不含氧元素;
(3)反应装置内还有一定量的水蒸气,所以步骤Ⅲ通入氨气的目的之一是排出装置内生成物,减小误差;
(4)碱石灰具有吸水性,如果略去装置B,会使水蒸气进入D装置内,D装置增加的质量会变大,
①装置C中不会发生新的化学反应,故①错误;
②会得出“氨气的组成中含有氧元素”的结论,故②正确;
③使测得的氨气组成中N、H元素质量比偏大,该实验是测量氧元素,然后进行比较的,故③错误;
故选:②;
(5)液面不平会产生压强,所以为减小误差,在读取量气管读数前必须进行的操作是:调节水准管,使量气管与水准管液面相平;
(6)题中的反应原理是通过比较C、D装置中氧元素的质量来判断的,所以氧化铜是否完全反应,对实验结果没有影响。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热在相同温度下,比较两组实验产生O2的快慢.
I中反应的化学方程式是_________;
II中x的值为________.
②乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
I | 50.0g | 1% | 0.1g | 9mL |
II | 50.0g | 2% | 0.1g | 16mL |
III | 50.0g | 4% | 0.1g | 31mL |
实验结论:在相同条件下,_______,双氧水分解得快.丙用如图装置进行实验,通过比较_______也能达到实验目的.

③某兴趣小组按照课本设计的实验(甲)探究分子的性质时,闻到了一股刺激性的气味,于是对原装置进行了改进。请回答:

(1)实验(乙)中观察到的现象是__________;
(2)兴趣小组改进的实验(乙),与实验(甲)相比的优点是________
【题目】同学们利用"硫酸、硝酸铵、氢氧化钠、碳酸钾"四种物质的溶液进行探究学习,完成下列各问:
(实验探究)
(1)A、B、C、D四组同学分别进行了下列实验
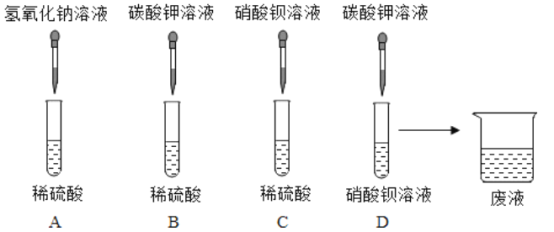
写出下列的两个化学方程式:
①A中的反应 ____________;
②D中的反应_____________ 。
(挖掘实质)
如下图是A组反应的微观过程示意图,该化学反应的实质可以表示为:H++OH-=H2O
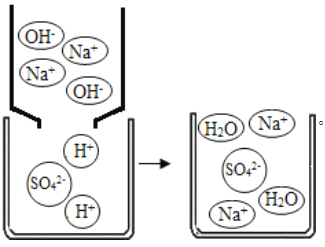
(实践运用)
(1)完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
(2)①溶液中的白色沉淀一定是________,理由是____________________
(3)废液中一定不含有的离子是_____和_________ 。
(4)为了验证该溶液中能会含有的离子是否存在,我设计如下实验进行验证:
溶液中可能含有的 离子 | 实验步骤 | 实验现象 | 实验结论 |
①_______________。 | ②取滤液滴加_______。 | 现象明显 | 含有该离子 |