题目内容
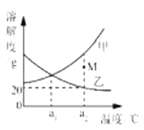
【题目】分析图中KNO3、NaCl两种固体的溶解度曲线,回答下列问题。
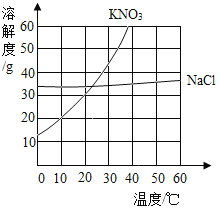
(1)在35℃时NaCl的溶解度_______(选填“大于”“等于”“小于”)KNO3的溶解度。
(2)20℃时将25gKNO3放入100g水中充分搅拌,得到该溶液的质量为______g。
(3)10℃时将10gNaCl和30gKNO3加入到100g的水中,充分搅拌。发现有固体剩余,则剩余的固体是_______(不考虑两物质对溶解性的影响);
(4)硝酸钾溶液中混有的少量氯化钠,提纯硝酸钾可采取_______(选填“降温结晶” 或“蒸发结晶”)。
【答案】小于 125 硝酸钾 降温结晶
【解析】
(1)从溶解度曲线图可得,35℃时NaCl的溶解度低于KNO3的溶解度,故填:小于。
(2)从溶解度曲线图可得,20℃时KNO3的溶解度为30g,因此20℃时将25gKNO3放入100g水中充分搅拌,全部溶解,形成125g溶液,故填:125。
(3)从溶解度曲线图可得,10℃时KNO3的溶解度为20g,NaCl的溶解度大于30g,因此10℃时将10gNaCl和30gKNO3加入到100g的水中,10gNaCl全部溶解,30gKNO3只能溶解20g,由10gKNO3固体未溶解,故填:硝酸钾。
(4)从溶解度曲线图可分析,硝酸钾的溶解度随温度变化影响较大,氯化钠的溶解度受温度影响较小,当硝酸钾溶液中混有的少量氯化钠时,可以采用降温结晶的方法提纯,降低温度,硝酸钾会以晶体形式析出,氯化钠受温度影响较小,且量小不是饱和溶液,不能析出晶体,达到分离除杂的目的。故填:降温结晶。

【题目】利用物质的性质能帮助我们开展科学探究。
[认识物质]
俗名 | 所含原子团 | 用途 | |
氢氧化钠 | _________、 火碱、苛性钠 | 氢氧根 | 精炼石油等 |
碳酸钠 | 纯碱、苏打 | ____ | 生产玻璃制品等 |
[定性检测]
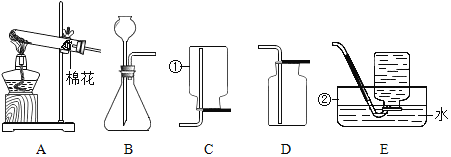
为检测久置空气中的氢氧化钠是否变质,设计并进行了如下图的实验:
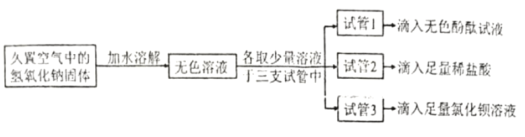
①试管1中观察到的现象是__________。
②试管2中观察到产生气泡,反应的化学方程式为___________。
③试管3中观察到产生__________。
④能达到实验目的的是试管__________(选填“1”、 “2”或“3”) 中的实验。
⑤若要判断氢氧化钠是部分变质还是全部变质,请你选择上述实验后三支试管中的液体继续实验,完成下表。
试管的编号 | 实验操作 | 现象和结论 |
试管________(选填“1”、“2”或“3”) | ____ | ____ |
[定量测定]
为了测定ag变质氢氧化钠中碳酸钠的质量分数,设计了如下的实验方案(浓硫酸具有吸水性):
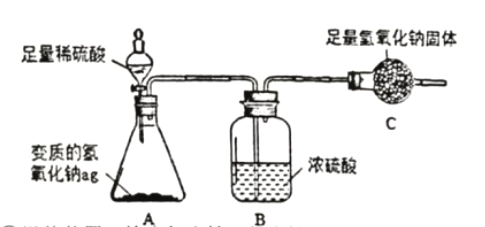
实验步骤和数据:①组装装置,检查气密性(气密性良好);②加入药品,称量C处装置质量为bg,滴入足量稀硫酸;③完全反应后称暈C处装置质量为cg;④后续处理。
实验分析:
I.判断碳酸钠已完全反应的实验现象是____________________。
II.利用实验数据,可得变质氢氧化钠中碳酸钠的质量分数为____________(用字母表示)。
Ⅲ.所得实验结果存在一定的误差, 可能的原因是_____________(写出一点即可)。