题目内容
【题目】水是生命之源,“珍惜水、节约水、 保护水”是每个公民的义务和责任。
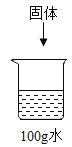
(1)天然水多为硬水,生活中可通过_______使其转化为软水。
(2)家用净水剂中常使用__________净水,可以吸附水中的异味和色素。
(3)如图为实验室电解水的装置,通电一段时间后,a管和b管中产生气体的体积比是____,反应的化学方程式为__________,该反应的基本类型是_________。
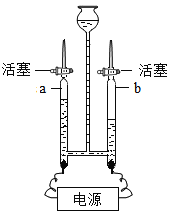
(4)爱护水资源,一方面要节约用水,另一方面要防治水体污染。水体污染的来源主要有工业污染、农业污染和__________。
【答案】煮沸 活性炭 1∶2 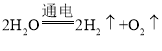 分解反应 生活污染
分解反应 生活污染
【解析】
(1)硬水中的可溶性钙镁化合物受热易分解生成难溶于水的水垢,从而降低水的硬度,因此生活中常用煮沸的方法降低水的硬度;
(2)活性炭具有吸附性,故家中净水常使用活性炭吸附水中的色素和异味;
(3)如图为实验室电解水的装置,通电一段时间后,a管中产生的气体较少,为氧气,b管中产生的气体较多,为氢气,a管和b管中产生气体的体积比是:1∶2,反应的化学方程式为: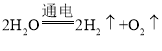 ,该反应由一种物质分解生成了两种物质,属于基本反应类型中的分解反应;
,该反应由一种物质分解生成了两种物质,属于基本反应类型中的分解反应;
(4)如果人类日常生活中产生的污水不经处理直接排放,也会造成水体污染,故水体污染的来源主要有工业污染、农业污染和生活污染。

【题目】已知:20℃时,KCl和KNO3的溶解度分别为34 g和31.6 g。配制20℃时的如下四种溶液:
| 溶液 | ① | ② | ③ | ④ |
固体种类 | KCl | KCl | KNO3 | KNO3 | |
加入固体的质量/g | 20 | 35 | 20 | 35 | |
水的质量/g | 100 | 100 | 100 | 100 |
下列有关溶液①~④的说法不正确的是
A.属于饱和溶液的是②④
B.溶液的质量②=④
C.溶液中溶质的质量分数①=③
D.②中溶质与溶剂的质量比为17:50
【题目】阅读下面科普短文。
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物。其实你真的了解SO2吗?难道它只是有害物质吗?
SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业。葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动。食糖加工过程中可使用SO2进行脱色。按照我国《食品添加剂使用标准(GB2760—2014)》,合理使用SO2不会对人体健康造成危害。
标准中部分食品SO2的最大残留量
食品 | 蜜饯 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
最大残留量 | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.1g/kg | 0.1g/kg | 0.05g/kg |
SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化。工业利用硫制硫酸的主要过程示意如下:
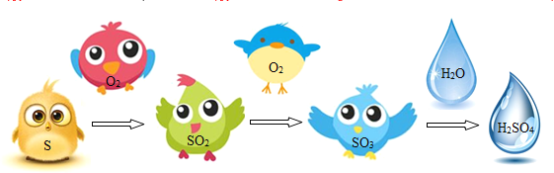
硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨。工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用。
SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2。为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量,改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理;还可以采取“优化能源结构、减少燃煤使用”的措施,例如,北京大力推广的“煤改气、煤改电”工程,有效改善了空气质量。
现在,你对SO2一定有了新的认识,在今后的化学学习中你对SO2还会有更全面的认识!
依据文章内容回答下列问题。
(1)按照国家标准,食糖中的SO2最大残留量为____________ g/kg。
(2)葡萄酒酿制过程中SO2的作用是_________。
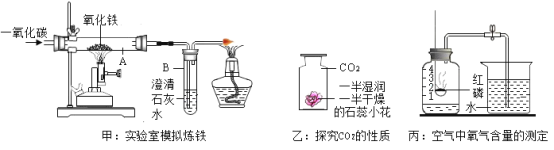
(3)用硫制硫酸的主要过程中,涉及到的含硫物质有S、_________和H2SO4。
(4)硫酸工业生产中,用SO3与水反应生产硫酸,发生反应的化学方程式为:_________;尾气中含有SO2气体污染空气,工业上可用___________处理尾气。
(5)下列措施能减少SO2排放的是__________(填序号)。
A 将煤块粉碎
B 对燃煤进行脱硫
C 推广煤改气、煤改电
D 循环利用工业尾气中的SO2
【题目】甲同学对有关盐的知识进行了以下的整理.
(1)填写下表空格中的化学式:
氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
______ | CaCl2 | NaCl | MgCl2 | AlCl3 | ______ | ______ | ______ |
反思:①以上盐中的金属元素的排列,可以得出是依据____顺序归纳整理的.
②酸在水溶液中能解离出共同的H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出共同的OH-,因此碱溶液也具有相似的化学性质.请据此分析上述盐溶液是否会具有相似的化学性质?____为什么?_____
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成图.验证:请写出下列有盐生成的部分化学方程式:
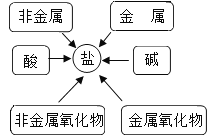
①用稀硫酸除铁锈_____;
②盐酸和氢氧化钠反应_____;属于____反应
③古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,化学方程式为_____;属于_____反应.
(3)甲同学在整理碳酸盐知识时,探究实验室用碳酸钙粉末、碳酸钠或碳酸氢钠,制取CO2的方法.
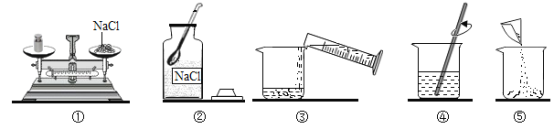
提出问题:实验室通常使用下列装置![]() 制取二氧化碳,此装置不适合用碳酸钙粉末、碳酸钠或碳酸氢钠作反应物的原因是_____.
制取二氧化碳,此装置不适合用碳酸钙粉末、碳酸钠或碳酸氢钠作反应物的原因是_____.
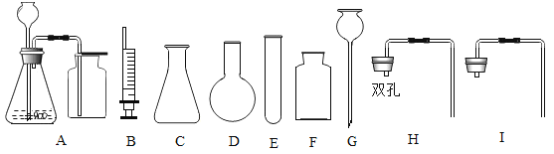
实验设计:通过控制反应物的用量来得到平稳的CO2气流的目的.因此,用碳酸盐粉末制取CO2的发生装置,可以选择_____(填仪器编号)组装.
(4)向16.8g碳酸氢钠粉末中,缓缓加入100g稀盐酸,如恰好完全反应,计算生成CO2的质量和反应前稀盐酸中溶质的质量分数_____.(请在答卷纸上写出计算过程)