题目内容
【题目】随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。
(1)在汽车电路中,经常用铜作导线,这是利用了铜的_________性。
(2)车体多用钢材制造。其表面喷漆不仅美观,而且可有效防止与______________接触而生锈。
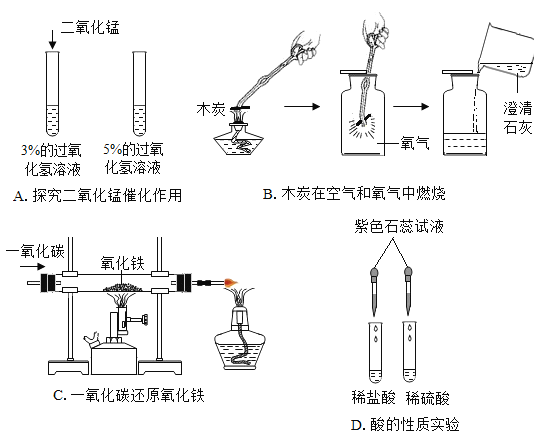
(3)工业上用CO还原赤铁矿冶炼金属铁的化学方程式为____________________________。
(4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是________________。(填一种即可)
【答案】导电 氧气和水或空气和水(或H2O和O2接触) 3CO+Fe2O3![]() 2Fe+3CO2(未配平或无条件扣1分,化学式错误扣2分) 稀盐酸或稀硫酸或硫酸铜溶液等(其他合理答都可)
2Fe+3CO2(未配平或无条件扣1分,化学式错误扣2分) 稀盐酸或稀硫酸或硫酸铜溶液等(其他合理答都可)
【解析】
(1)铜作导线是因为铜有良好的导电性;
(2)车体多是铁合金,易与空气中水和氧气反应而生锈,涂漆不仅美观而且也能防锈;
(3)赤铁矿的主要成分是氧化铁,氧化铁与一氧化碳在高温条件下生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(4)判断金属活动性,可利用金属与酸反应的现象,或金属与盐溶液之间的反应现象来判断。在金属活动性顺序中,排在氢前面的金属会与酸反应生成氢气,所以在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是稀盐酸或稀硫酸或可溶铜盐溶液或可溶铝盐溶液,故填:稀盐酸或稀硫酸或硫酸铜溶液。

【题目】小冬在课外阅读中得知:氢氧化铜受热会分解生成氧化铜和水,于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
(1)请写出加热氢氧化铜的化学方程式为____________________。
(2)小冬在加热氢氧化铜时,发现蓝色固体先变成黑色;继续高温灼烧黑色固体变成红色,同时有气体产生。为弄清这种红色固体的成份,进行了如下的探究:
(查阅资料)Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
(提出猜想)红色固体是:Ⅰ.Cu Ⅱ.Cu2O Ⅲ.______________。
(进行实验)
操作 | 现象 | 结论 |
①取灼烧后的红色固体2g于试管中,加入足量稀硫酸,加热并充分振荡,静置。 | _________________ | 红色固体中含有Cu2O |
②过滤、洗涤、干燥。 | 得红色固体 | 红色固体中含有Cu |
(结论分析)据上述现象,小冬认为猜想______成立。你认为小冬的结论是否合理______(填“是”或“否”),理由是_______________________________________。如要证明红色固体的成分,还需要补充的操作是________________________________________。