题目内容
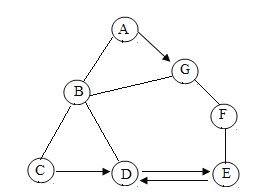
【题目】已知 A、B、C、D 是初中化学中常见的四种不同类别的物质,A 是一种经过一系列复杂变化形成的红色固体,用“—”表示物质之间可以相互反应,用“→”表示一种物质可以转化生成另一种物质(部分反应物、生成物和反应条件已略去)。 请回答下列问题:
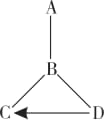
(1)A 的化学式:_______________。
(2)写出 A-B 反应的化学方程式:_____________,工业上该反应可应用于______________。
(3)写出 D→C 反应的化学方程式:_______________。
【答案】Fe2O3 ![]() 除铁锈
除铁锈 ![]() [或
[或 ![]() 或
或![]() ]
]
【解析】
A 是一种经过一系列复杂变化形成的红色固体,所以A为氧化铁;A、B、C、D 是初中化学中常见的四种不同类别的物质,A(氧化铁)能与B发生化学反应,所以B应为酸类,即B为盐酸或硫酸;A、B、C、D 是初中化学中常见的四种不同类别的物质,B(酸)能与碱或盐反应,且盐、碱可以相互转化,则C、D为碱或盐,且C、D均能与B(酸),所以C与D可以分别为碳酸钠与氢氧化钙,或氢氧化钙与碳酸钙,或氢氧化钠与碳酸钠等。
(1)由分析可知,A为氧化铁,其化学式为Fe2O3,故填Fe2O3。
(2)由分析可知,B为酸,可为盐酸,氧化铁与盐酸反应生成氯化铁和水,故反应的化学方程式写为:Fe2O3+6HCl=2FeCl3+3H2O;
酸与金属氧化物反应生成盐与水,所以可以利用该原理除锈,故填除锈。
(3)由分析可知,C与D可以分别为碳酸钠与氢氧化钠,或氢氧化钙与碳酸钙,或氢氧化钠与碳酸钠,所以D→C 反应是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,D→C 反应还可能是氢氧化钙氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O,D→C 反应还可能是氢氧化钠与二氧化碳反应生成碳酸钠和水,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O,故填Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或Ca(OH)2+CO2=CaCO3↓+H2O或2NaOH+CO2=Na2CO3+H2O等。

【题目】过一硫酸氢钠复合盐(Na2SO4·NaHSO4·2NaHSO5)是一种新型酸性过氧化物消毒剂。以过氧化氢溶液、浓硫酸、碳酸钠为原料制备过一硫酸氢钠复合盐的一种工艺流程如下:

注:过一硫酸(H2SO5)在常温下为无色晶体,熔点 45℃,易溶于硫酸溶液中,可与水缓慢反应生成硫酸与过氧化氢,受热易分解。
(1)碳酸钠的俗名为________。过一硫酸氢钠复合盐中共含有_________种元素。
(2)中和过程中有如下反应发生:Na2CO3 + H2SO4 = Na2SO4 + X↑+ H2O。气体 X的化学式为_________。
(3)在合成过一硫酸时,反应温度应控制在-4℃左右的主要原因是_____。
(4)固定H2O2的用量,以H2O2与H2SO4的质量比、中和温度及所加 Na2CO3 的质量为变量,可探究上述三种因素对复合盐产量的影响(见下表)。
实验序号 | H2O2 与 H2SO4 质量比 | 中和温度/℃ | Na2CO3 用量/g |
① | 47.6 : 29.8 | 7 | 23.0 |
② | 47.6 : 33.6 | 10 | 25.0 |
③ | 47.6 : 25.3 | 4 | 21.5 |
④ | 47.6 : 29.8 | 10 | 23.0 |
⑤ | 47.6 : 25.3 | 7 | 21.5 |
上述实验中,可用来探究中和温度对复合盐产量影响的是__________(填字母)。
a 实验①、④ b 实验②、③ c 实验③、④ d 实验③、⑤
(5)在双氧水定量的基础上,所用硫酸溶液中溶质的质量分数与复合盐中活性氧含量的关系见下图。

①验过程中选用质量分数为55%左右的硫酸溶液,主要原因是_______。
②配制 98g 质量分数为55.2%的硫酸溶液所需质量分数为 98%的硫酸溶液(密度约为1.84g/cm3)的体积为_______mL。