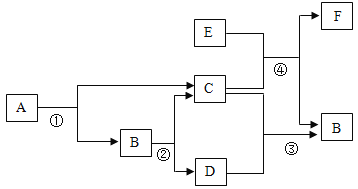
题目内容
【题目】向 100 克 MgCl2 和 HCl 的混合溶液中,逐滴加入 10%的氢氧化钠溶液,反应情况,如图所示。

(1)当滴加氢氧化钠溶液的质量至 N 点时所得溶液的 pH 值为_______(填编号);
A大于 7 B等于 7 C小于 7
(2)通过计算,确定 M 点时所得溶液中溶质的质量分数,写出计算过程____。
【答案】A 9.2%(详见解析)
【解析】
向 100 克 MgCl2 和 HCl 的混合溶液中,逐滴加入 10%的氢氧化钠溶液,氢氧化钠先与盐酸反应,等盐酸完全反应后再与氯化镁反应。
(1)当滴加氢氧化钠溶液的质量至N点时,氢氧化钠过量,溶液呈碱性,pH.>7,故选A;
(2)根据图示可知,反应过程中生成了5.8g的氢氧化镁。
设恰好完全反应时,和氯化镁反应的氢氧化钠溶液的质量为x
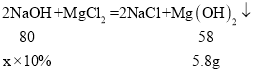
![]()
x=80g
所以反应的全部的氢氧化钠的质量为(80g+80g)×10%=16g;
设生成的氯化钠的质量为y,由于钠元素最终转到氯化钠得关系式为:
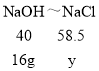
![]()
y=23.4g
所得氯化钠溶液中氯化钠的质量分数为![]() 。
。
答:当加入10%的氢氧化钠溶液的质量为M时溶液中氯化钠的质量分数为9.2%。

 阅读快车系列答案
阅读快车系列答案【题目】关于下列事实的解释不正确的是( )
选项 | 事实 | 解释 |
A | 10mL酒精和10mL水混合后体积小于20mL | 分子之间有间隔 |
B | 稀硫酸和稀盐酸化学性质相似也存在差异 | 溶液中都含有H+ , 也存在不同的SO42-、Cl-离子 |
C | 酒精溶液不导电 | 溶液中没有自由移动的带电粒子 |
D | 化肥硫酸铵不能和熟石灰混放或混用 | 硫酸铵与熟石灰发生中和反应 |
A.A B.B C.C D.D
【题目】某化学兴趣小组在实验室实验时发现一瓶标签缺损的溶液,如图,为了确定其溶质成分,同学们进行了如下探究:
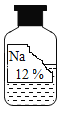
(提出猜想)
猜想一:NaCl;
猜想二:Na2CO3;
猜想三:NaHCO3;
猜想四:NaOH。
(设计实验一)小明取少量溶液样品于试管中 ,用玻璃棒蘸取溶液滴在pH试纸上,读取数据:pH=9,得出结论:猜想四成立。
小王认为小明的结论不准确,理由是___________________。从小明的实验结果中可以判断猜想____一定是错误的。
(设计实验二)小红取适量稀盐酸于试管中,滴加少量此溶液,溶液中产生气泡。于是认为猜想二正确。小王认为仍然不能确定,理由是______________ (用化学方程式解释)
(查阅资料)常温下,碳酸钠和碳酸氢钠溶解度如下表:
物质 | 碳酸钠 | 碳酸氢钠 |
溶解度/g | 21.8 | 9.6 |
(分析结论)
从资料显示的数据,再结合药品的标签可以判断猜想三不正确,理由是______________________。
(交流讨论)
(1)碳酸钠和碳酸氢钠在生活中被称为“苏打兄弟”,其中NaHCO3在生活中可用来___________(写一条即可)
(2)碳酸钠在空气中长期放置,会吸收空气中的水蒸气和另一种气体而转变成碳酸氢钠,另一种气体是_____________。