题目内容
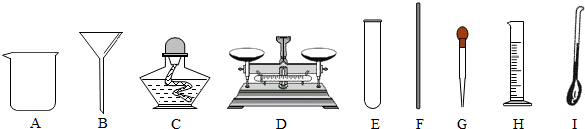
某同学在配制50g溶质量分数为5%的食盐溶液的实验中,称量时将砝码放在左盘(1g以下用游码),食盐放在右盘;量水时仰视液面读数.这样配制的食盐溶液中的质量分数( )A.等于5%
B.大于5%
C.小于5%
D.不能确定
【答案】分析:使用托盘天平时应把称量物放在左盘,若放在右盘且使用游码则实际质量为砝码-游码,量取水时,应平视凹液面最低处,若仰视则水多,俯视则水少.
解答:解:配制50g溶质量分数为5%的食盐溶液,需要食盐2.5g,将砝码放在左盘(1g以下用游码),食盐放在右盘,则食盐的实际质量为2g-0.5g=1.5g,水47.5mL,量水时仰视液面读数则导致水的体积大于47.5mL,溶质少了,水多了,故溶液变稀,其溶质质量分数小于5%,故选C.
点评:配制溶液时,要按照正确的操作进行称量,要知道错误操作对实验结果的影响.
解答:解:配制50g溶质量分数为5%的食盐溶液,需要食盐2.5g,将砝码放在左盘(1g以下用游码),食盐放在右盘,则食盐的实际质量为2g-0.5g=1.5g,水47.5mL,量水时仰视液面读数则导致水的体积大于47.5mL,溶质少了,水多了,故溶液变稀,其溶质质量分数小于5%,故选C.
点评:配制溶液时,要按照正确的操作进行称量,要知道错误操作对实验结果的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
烧碱(NaOH)是一种重要的化工原料,广泛应用于肥皂、造纸等工业.下面有一些关于烧碱的问题,请按要求解答:
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式 .
(2)烧碱放在空气中会变质生成碳酸钠.现有14.6g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10g沉淀,则样品的组成为 .
A.全部为Na2CO3
B.4g NaCO3和10.6g NaOH
C.全部为NaOH
D.4g NaOH和10.6g Na2CO3
(3)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到明显现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应. .
(4)若中和反应需要60g 10%的NaOH溶液,现提供50g 20%的NaOH溶液、40g 5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品设计两种配制方案(只要说明配制所需的各种药品用量)填入表中.
a(5)如图是某学生用氢氧化钠固体和水配制60g10%NaOH溶液的部分操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量.
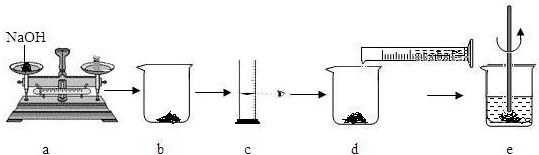
①a操作中的错误是 .
②下列操作中导致溶质质量分数偏低的是 (填字母).
A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50mL
D.d操作中有少量水溅出.
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式
(2)烧碱放在空气中会变质生成碳酸钠.现有14.6g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10g沉淀,则样品的组成为
A.全部为Na2CO3
B.4g NaCO3和10.6g NaOH
C.全部为NaOH
D.4g NaOH和10.6g Na2CO3
(3)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到明显现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应.
(4)若中和反应需要60g 10%的NaOH溶液,现提供50g 20%的NaOH溶液、40g 5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品设计两种配制方案(只要说明配制所需的各种药品用量)填入表中.
| 序号 | 配置方案 |
| 举例 | 6gNaOH固体和54g水 |
| 方案1 | |
| 方案2 |

①a操作中的错误是
②下列操作中导致溶质质量分数偏低的是
A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50mL
D.d操作中有少量水溅出.