题目内容
【题目】已知M、N分别是稀盐酸、氢氧化钠溶液中的一种。某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示。
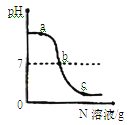
(1)N是 ,b点表示的意义是 反应的化学方程式为 ,所属基本反应类型是 反应。
(2)据图分析c处溶液中的阳离子有 、 (填写离子符号)。
【答案】(1)稀盐酸 盐酸与氢氧化钠恰好反应。 HCl+NaOH===NaCl +H2O 复分解 (2)Na+、H+
【解析】
试题分析:根据图示看N点的PH值小于7,使用N是盐酸,b点的PH值等于7表示的意义是盐酸与氢氧化钠恰好反应。反应的化学方程式HCl+NaOH===NaCl +H2O;属于复分解反应;据图分析c处溶液中酸还没有反应完,但是反应了一定的时间了所以其中的阳离子有Na+、H+。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目