题目内容
【题目】城铁助力青烟威经济腾飞,关于城铁、动车有下列问题,请回答
(1)合金性能优于单一金属,因而被广泛应用,焊锡(主要含锡、铅)与其组成金属相比具有_______的特性,可用于焊接电子元件。
(2)电车的坐骑和拉手制作时使用的大量塑料属于_______材料。
(3)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀,为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,由此可知该零件“发蓝”处理效果_______(填“好”或“不好”),因为_______(用化学方程式表示)。
(4)高铁建设需要消耗大量的铝、铁等金属
①工业上常用电解氧化铝的方法冶炼金属铝,该反应属于_______(填字母序号)
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
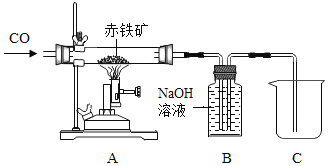
②某兴趣小组在实验室中利用CO气体模拟炼铁的原理,如图所示。
Ⅰ.为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应_______。
Ⅱ.装置A玻璃管中发生反应的化学反应方程式是_______。
Ⅲ.装置B的作用是_______。
【答案】熔点低 有机合成 不好 Fe+CuSO4=FeSO4+Cu B 先通入一氧化碳 3CO+Fe2O3![]() 2Fe+3CO2 吸收二氧化碳,收集未反应的一氧化碳。
2Fe+3CO2 吸收二氧化碳,收集未反应的一氧化碳。
【解析】
(1)合金的熔点一般低于成分金属,焊锡(主要含锡、铅)与其组成金属相比具有熔点低的特性,可用于焊接电子元件,故填熔点低。
(2)电车的坐骑和拉手制作时使用的大量塑料属于有机合成材料,故填有机合成。
(3)零件表面出现红色物质,是因为裸露的铁与硫酸铜反应生成了硫酸亚铁和铜,说明该零件“发蓝”处理效果不好,故填不好;
铁与硫酸铜反应生成硫酸亚铁和铜,故反应的化学方程式写为:Fe+CuSO4=FeSO4+Cu。
(4)①工业上常用电解氧化铝的方法冶炼金属铝,同时生成氧气,该反应属于分解反应,故填B;
②Ⅰ.为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应先通入一氧化碳,排尽装置内的空气,故填先通入一氧化碳。
Ⅱ.装置A玻璃管中一氧化碳和氧化铁再高温的条件下反应生成铁和二氧化碳,故反应的化学方程式写为:3CO+Fe2O3![]() 2Fe+3CO2。
2Fe+3CO2。
Ⅲ.装置B在好的氢氧化钠能吸收二氧化碳,收集未反应的一氧化碳,故填吸收二氧化碳,收集未反应的一氧化碳。

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案【题目】实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小明用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如表,请分析计算(写出计算过程)
实验组别 | 一 | 二 | 三 | 四 |
稀盐酸质量/g | 100.0 | 100.0 | 100.0 | 100.0 |
混合物质量/g | 3.0 | 6.0 | 9.0 | 12.0 |
所得溶液质量/g | 101.9 | 103.8 | 105.0 | a |
剩余固体质量/g | 0 | 0 | m | n |
(1)求混合物中碳酸钙和氯化钙质量之比__________
(2)表中a的值为_______。
(3)求表中m的值__________。
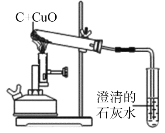
【题目】碳还原氧化铜的实验如右图所示。写出该反应的化学方程式____。
(提出问题)碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
(作出猜想)猜想①:CO
猜想②:CO2
想③:____________。
(设计方案)实验装置如图(浓硫酸具有吸水作用)。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
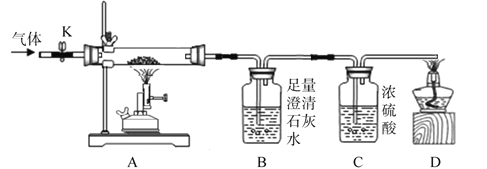
方案一:从定性观察角度判断
(1)实验时A处的现象是____________。
(2)若猜想①成立,B、D处的现象是_____________(填序号)。
a.B中变浑浊,D处能点燃 b.B中变浑浊,D处不能点燃
c.B中无明显实验现象,D处能点燃 d.B中无明显实验现象,D处不能点燃
方案二:从定量计算角度判断
取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
A(玻璃管+固体) | m1 | m2 |
B+C(广口瓶+混合液) | m3 | m4 |
(3)若猜想②成立,则理论上(m4-m3)__(m1-m2)(选填“<”、“>”或“=”)。
(4)若猜想③成立且CuO全部转化成Cu,则参加反应的碳的质量m的取值范围是____。
(交流反思)实验开始前缓缓通入氮气的目的是____。