题目内容
【题目】实验室用硫酸铜(不含结晶水)作过氧化氢溶液制取氧气的催化剂。现在2.0g硫酸铜中加入34.0g过氧化氢溶液,充分反应后,实验的相关数据如图。(不考虑反应过程中水分的蒸发),请计算:
(1)制得氧气的质量为_____g。
(2)过氧化氢溶液中溶质的质量分数为多少_____?(写出计算过程)。
(3)反应后所得硫酸铜溶液的溶质质量分数为_____(精确到0.1%)。

【答案】0.8 5% 5.7%
【解析】
根据质量守恒定律可得,生成的氧气的质量为36g﹣35.2g=0.8g
设过氧化氢溶液中溶质的质量分数为x
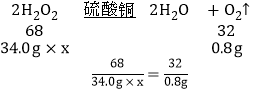
x=5%
反应后所得硫酸铜溶液的溶质质量分数为![]() ×100%=5.7%。
×100%=5.7%。
故答案为:
(1)0.8;
(2)5%;
(3)5.7%。

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
【题目】如图是实验室制取气体的常用装置,请根据图回答下列问题。
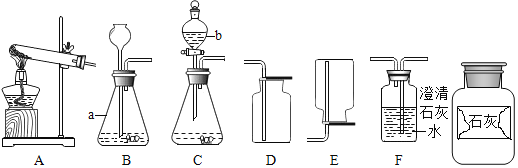
(1)写出图中标有序号的仪器名称:a______;b______。
(2)若使用装置A制取氧气,应______(填改进措施)方可继续实验,其化学方程式是______。
(3)某广口瓶上的标签已破损,只剩下“石灰”两个字,已知该样品未变质。某兴趣小组设计实验探究该药品的成分,请完成以下实验报告。
实验步骤 | 实验现象 | 结论 |
取少量瓶中的固体于烧杯中,加入适量水,并感知烧杯壁的温度 | ______ | 固体不是生石灰 |
取上述烧杯中的少量上层清液于试管中,滴加酚酞试液 | 无明显现象 | 固体不是熟石灰 |
取少量瓶中的固体于装置B中,加入适量稀盐酸 | 产生大量气泡,装置F中的澄清石灰水变浑浊 | F中涉及化学方程式为 ______ |
(4)确定药品的成分后,兴趣小组选用了图中的______(填序号),可实现控制反应的发生与停止。