题目内容
【题目】根据下列图示,回答相关问题。

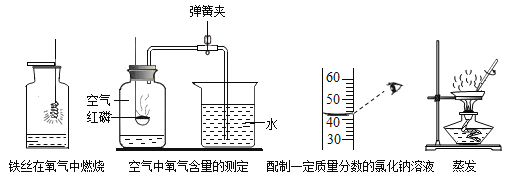
(1)写出仪器①的名称:_________________。
(2)实验一中的收集装置不能用于收集氢气的原因是_________________,该装置中的分液漏斗相比于长颈漏斗具有的显著优点是_________________。
(3)实验二:刚开始加热时,澄清石灰水中有气泡产生,而澄清石灰水不变浑浊,其原因是___________,木炭还原氧化铜的化学方程式为______________。
【答案】集气瓶 氢气密度比空气密度小,不能用向上排空气法收集 可以控制反应速率 加热时空气体积膨胀,先排出了空气 
【解析】
(1)仪器①是集气瓶;故填:集气瓶;
(2)氢气密度比空气密度小,不能用向上排空气法收集,所以实验一中的收集装置不能用于收集氢气;该装置中的分液漏斗可以通过控制液体的滴加速率来控制反应的速率。故填:氢气密度比空气密度小,不能用向上排空气法收集;可以控制反应速率;
(3)实验二:刚开始加热时,空气体积受热膨胀,先排出空气,澄清石灰水中有气泡产生,而澄清石灰水不变浑浊;木炭和氧化铜在高温条件下反应生成铜和二氧化碳,反应的化学方程式为 。故填:加热时空气体积膨胀,先排出了空气;
。故填:加热时空气体积膨胀,先排出了空气; 。
。

 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案【题目】小云同学完成如图实验:向盛满CO2气体的塑料瓶中加入澄清的石灰水,拧紧瓶盖振荡。让她吃惊的是瓶子虽然变瘪了,但是并没有看到白色沉淀。

(发现问题)沉淀哪去了?
(探究环节一)
提出猜想:二氧化碳没有和氢氧化钙反应,而是直接溶于水了。于是设计如下实验进行验证。
步骤 | 操作 | 实验现象 |
1 | (1)取2个相同规格的软塑料瓶, 分别集满二氧化碳气体 (2)分别向 2 个塑料瓶中注入等体积的氢氧化钙溶液和蒸馏水, 拧紧瓶盖,振荡 | 2 个塑料瓶都变瘪了,但是注入氢氧化钙溶液的塑料瓶瘪的程度更大 |
2 | (1)用pH试纸测反应前氢氧化钙溶液的酸碱度 (2)向软塑料瓶中注入适量氢氧化钙溶液震荡后,测反应后溶液的 pH 值 | 反应前氢 氧 化 钙 溶 液 的 pH 大于 7; 反应后 溶液的pH小于7 |
(1)小云预期会看到白色沉淀的依据是______________________(写出反应的化学方程式)
(2)反应后溶液的pH小于7是由于生成了____(写化学式);通过分析以上实验现象,小云得到的结论是_______________________。
(探究环节二)
查阅资料后得知:适量的二氧化碳和氢氧化钙能发生反应生成难溶于水的碳酸钙,如果二氧化碳过量,则碳酸钙会继续和二氧化碳反应生成可溶性的碳酸氢钙。(“→”代表反应的方向)CO2+CaCO3+H2O ![]() Ca(HCO3)2
Ca(HCO3)2
提出猜想:实验中可能二氧化碳过量,反应生成了碳酸氢钙,所以没有看到沉淀
步骤 | 操作 | 实验现象 |
1 | 取少量的氢氧化钙溶液于试管中,向其中持续通入CO2气体 | 开始产生白色沉淀过一会儿,白色沉淀消失 |
2 | (1)取一个软塑料瓶,集满二氧化碳气体,向其中注入少量的氢氧化钙溶液,拧紧瓶盖,振荡 (2)此时将软塑料瓶放在热水浴中加热 (3)将加热后的软塑料瓶冷却 | 瓶子变瘪 溶液变浑浊 溶液又变澄清 |
3 | (1)取一个软塑料瓶,集满二氧化碳气体,向其中注入少量的氢氧化钙溶液,拧紧瓶盖,振荡 (2)向实验后的软塑料瓶中继续滴加氢氧化钙溶液 | ? |
实验结论:猜想成立
(1)实验步骤2中“改变瓶子的温度”目的是___________。
(2)实验步骤3中看到的实验现象是________________。