题目内容
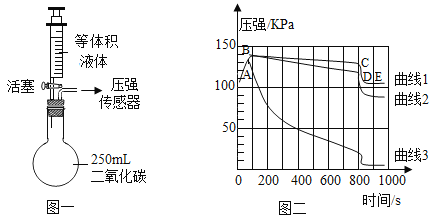
【题目】以甲为原料制取丁的反应微观示意图如下:

对该反应的分析中正确的是( )
A.转化①是分解反应,转化②是化合反应
B.转化①反应中甲、乙、丙的粒子个数比为 1∶1∶2
C.甲、乙、丁都属于有机物
D.转化②中乙、丁的质量比为 8∶7
【答案】B
【解析】
A、根据题中图示,乙分子中含有氧原子,而甲的分子中不含氧原子,故氧气是反应物,因此转化①的化学方程式是: ,反应物和生成物都是两种,不符合分解反应的特征,不属于分解反应;转化②的化学方程式是:
,反应物和生成物都是两种,不符合分解反应的特征,不属于分解反应;转化②的化学方程式是: ,反应物是两种,生成物是一种,符合化合反应的特征,属于化合反应。选项A不正确;
,反应物是两种,生成物是一种,符合化合反应的特征,属于化合反应。选项A不正确;
B、图中甲是CH4,乙是CO,丙是H2,根据转化①的化学方程式 ,化学方程式中化学式前的化学计量数之比就是参加反应的这些物质的粒子个数比,因此反应中甲、乙、丙的粒子个数比为 1∶1∶2,选项B正确;
,化学方程式中化学式前的化学计量数之比就是参加反应的这些物质的粒子个数比,因此反应中甲、乙、丙的粒子个数比为 1∶1∶2,选项B正确;
C、有机物都是含碳化合物,但少数含碳化合物如一氧化碳等具有无机物的特点,因此把它们看作无机物。故甲、丁是有机物,而乙是无机物,选项C不正确;
D、根据转化②的化学方程式是: ,乙和丁的质量比为:(2×28)∶(2×32)= 7∶8,选项D不正确。故选B。
,乙和丁的质量比为:(2×28)∶(2×32)= 7∶8,选项D不正确。故选B。

 口算能手系列答案
口算能手系列答案【题目】某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。查阅资料可知 Mg、Mg3N2能发生如下反应:
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。回答下列问题:
(1)连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是_____(填装置序号)。D装置中发生反应的化学方程式为_____。
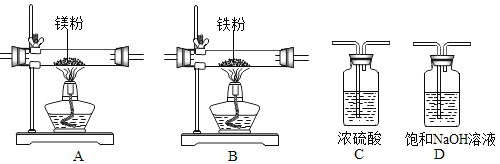
(2)通气后,应先点燃_____(填“A”或“B”)装置的酒精灯,如果同时点燃A、B装置的酒精灯,对实验结果有何影响?_____。
(3)设计一个实验,验证产物是氮化镁:
实验操作和实验现象 | 实验结论 |
_____ | 产物是氮化镁 |
(4)思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N2的质量,请给出合理的解释_____。
【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如右图),为确认其中的溶质,同学们进行了如下的探究活动。请你参与到其中去,回答有关问题。
【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想IV:该溶液的溶质是NaHCO3.
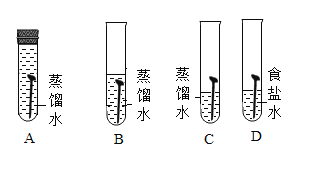
【查阅资料】常温下物质的相关信息如下表:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知,该溶液的溶质不是NaHCO3,因为常温下NaHCO3溶液溶质的质量分数最大是
(精确到01.%)。
【进行实验】
(1)测定溶液的pH大于7,该溶液的溶质不是 (填化学式)。
(2)同学们又进行了如下实验,实验过程如下:
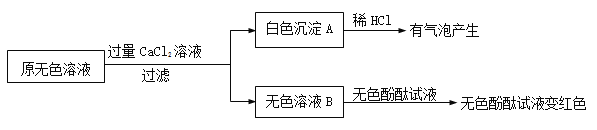
①产生白色沉淀的化学方程式是 。
②实验可以判断原无色溶液中含有的溶质有 。
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且 (填“没有”、“部分”或“全部”)变质。
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的 ,然后过滤。反应化学方程式是 。