题目内容
【题目】某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示:求:
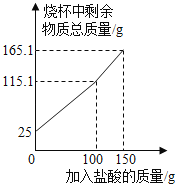
(1)产生CO2的总质量为_____g。
(2)鸡蛋壳中碳酸钙的质量分数_________。
(3)请在如图坐标中画出盐酸的质量和CO2质量之间的相应的曲线图____________(要求标出曲线中必要的数据)。
【答案】9.9 90% 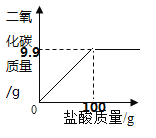
【解析】
解:(1)加入盐酸质量为100g时,溶液的质量为115.1g,加入盐酸质量为150g时,溶液的质量为165.1g,说明加入100g稀盐酸后溶液质量和不再改变,说明此时已经完全反应。根据质量守恒定律可得,生成的二氧化碳的质量为25g+100g-115.1g=9.9g
(2)设鸡蛋壳中碳酸钙的质量分数是x。
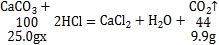
![]()
得:x=90%
(3)如图坐标中画出盐酸的质量和二氧化碳质量之间的相应的曲线图,起点是0,结束点是(100,9.9),之后水平,为: 。
。

 科学实验活动册系列答案
科学实验活动册系列答案【题目】某化学兴趣小组用实验室常用药品(或溶液)对 “NaOH 溶液与稀盐酸是否恰好完全反应”进行探究。
(知识卡片):氯化钠溶液显中性。氯化铜易溶于水。
(实验探究):
(1)方案I:某同学先向试管中加入约 2mL NaOH 溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论_____。
②从微观的角度分析,该反应的实质是_____。
(2)方案Ⅱ:
实验步骤 | 实验现象 | 结论 |
取 2mL NaOH 溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 | 若_____ | 稀盐酸过量 |
若没有明显现象 | NaOH 溶液与稀盐酸恰好完全反应 |
(实验反思):
(3)另有同学提出方案Ⅱ不能证明 NaOH 溶液与稀盐酸恰好完全反应,其原因是_____。
(4)除以上方案外,下列哪些物质单独使用,也能证明 “NaOH 溶液与稀盐酸是否恰好完全反应”_____(填序号)。
A铜片 BpH 试纸 C氧化铜 D紫色石蕊试液