题目内容
【题目】用等质量相同表面积的镁条、等体积不同浓度的稀盐酸在一定条件下反应,实验结果如图所示。下列结论正确的是
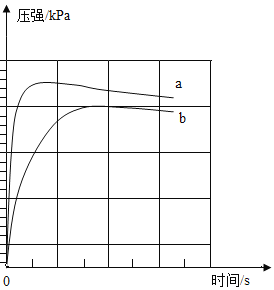
①镁与盐酸的反应是放热反应
②b曲线对应的盐酸浓度较大
③盐酸浓度越大,反应速率越快
④单位时间内放出热量越多,反应速率越快
⑤装置内氢气的质量先增大,后减小
⑥两种情况最终产生氢气的质量可能相同
A.①②③④B.①③④⑤C.①③④⑥D.③④⑤⑥
【答案】C
【解析】
①镁与盐酸反应生成氯化镁和氢气,该反应是放热反应,符合题意;
②盐酸的浓度越大,反应速率越快,压强增大越明显,故a曲线对应的盐酸浓度较大,不符合题意;
③盐酸浓度越大,反应速率越快,说法正确,符合题意;
④镁与盐酸反应放热,单位时间内放出热量越多,说明反应速率越快,符合题意;
⑤镁与盐酸反应生成氢气,随着反应的进行,氢气质量逐渐增加,待完全反应后,氢气的质量不再变化,故装置内氢气的质量先增大,后不变,不符合题意;
⑥如盐酸过量,镁条的质量相等,两种情况最终产生氢气的质量相同,符合题意。
正确的是:①③④⑥;故选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目