题目内容
【题目】钛(Ti)和钛合金是二十一世纪重要的金属材料,享有“未来金属”的美称,可用于制造航天飞机、船舶等。钛的冶炼方法很多,方法之一是利用二氧化钛和金属铝在高温条件下发生置换反应制得,该反应的化学方程式为_____,该反应中化合价升高的元素是_____,该反应中发生还原反应的物质是_____。
【答案】3TiO2+4Al![]() 3Ti+2Al2O3 铝 二氧化钛
3Ti+2Al2O3 铝 二氧化钛
【解析】
二氧化钛和金属铝在高温下反应生成钛和氧化铝。
二氧化钛和金属铝在高温下反应生成钛和氧化铝,化学方程式为 ;化合物中各元素化合价之和为零,在单质中,元素的化合价为零,反应前氧显﹣2价,钛显+4价,铝化合价为零,反应后氧显﹣2价,铝显+3价,钛的化合价为零,其中铝的化合价升高,二氧化钛中的氧被夺去,发生还原反应。
;化合物中各元素化合价之和为零,在单质中,元素的化合价为零,反应前氧显﹣2价,钛显+4价,铝化合价为零,反应后氧显﹣2价,铝显+3价,钛的化合价为零,其中铝的化合价升高,二氧化钛中的氧被夺去,发生还原反应。

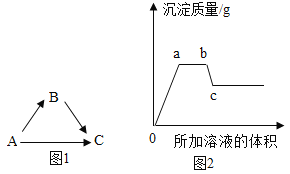
【题目】今年“五·一”假期,小丽随爸爸到乡下省亲,期间看到许多漂亮的大理石,于是好带了一些回来,想去学校实验室测定这此大理石中CaCO3的含量。他称取了20克大理石样品置于烧杯中,然后将250g稀盐酸分成五等份,依次加入烧杯充分反应,记录有关实验数据如下表所示(大理石中其他分均不溶于水,也不参与化学反应)。
加入次数 | 一 | 二 | 三 | 四 | 五 |
加入稀盐酸的质量 | 50 | 50 | 50 | 50 | 50 |
烧杯中剩余固体的质量 | 15 | 10 | 5 | 5 | m |
试求:(1)m的值应为_____;
(2)实验中大理石样品所含CaCO3的质量分数?_____
(3)实验中所用稀盐酸的溶质质量分数?_____
【题目】某班同学为验证碳酸钠的化学性质,向盛有碳酸钠的试管中加入一定量的稀盐酸,迅速用带导气管的橡胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中(如图所示)。请回答下列问题:
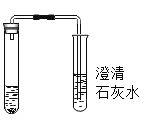
(1)右侧试管中澄清石灰水变浑浊,写出该反应的化学方程式_____。
(2)实验结束后,将两支试管中的所有物质倒入同一个废液缸中,充分反应后得到澄清溶液。同学们对废液中溶质的成分进行如下探究(忽略二氧化碳的影响):
(提出问题)
废液中溶质的成分是什么?
(做出猜想)
猜想一:CaCl2、NaCl和HCl
猜想二:CaCl2、NaCl和Na2CO3
猜想三:_____;
(进行讨论)
经过讨论,同学们一致认为猜想_____是错误的。
(设计实验)请完成实验报告
实验步骤 | 实验现象 | 实验结论 |
取少量废液于试管中,加入_____; | _____ | 猜想一成立 |
(反思拓展)
最终同学们确认了废液中溶质的成分。若将废液直接排入铸铁管道引起的危害是_____,你认为该废液的处理方法是_____。