题目内容
某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其他杂质不与盐酸反应)。
试计算:
(1)用10克30%的浓盐酸配制成2%的稀盐酸,需加水多少克?
(2)取20克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸7.3克,求废水中氢氧化钾的质量分数。
试计算:
(1)用10克30%的浓盐酸配制成2%的稀盐酸,需加水多少克?
(2)取20克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸7.3克,求废水中氢氧化钾的质量分数。
(1)140g (2)1.12%
依据“稀释前后溶质质量不变”列等式可以计算需要加水的质量;根据消耗的7.3 g 2%的稀盐酸即可求出20 g废水中氢氧化钾的质量,从而求出废水中氢氧化钾的质量分数。
解:(1)配制2%的稀盐酸的质量为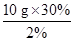 ="150" g,需要加水的质量为
="150" g,需要加水的质量为
150 g-10 g="140" g。
答:需加水140 g
(2)设参加反应的氢氧化钾的质量为x,
HCl + KOH=KCl+H2O
36.5 56
7.3 g×2% x
36.5∶56="(7.3" g×2%)∶x x="0.224" g
废水中氢氧化钾的质量分数为
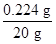 ×100%=1.12%
×100%=1.12%
答:废水中氢氧化钾的质量分数为1.12%。
解:(1)配制2%的稀盐酸的质量为
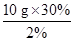 ="150" g,需要加水的质量为
="150" g,需要加水的质量为150 g-10 g="140" g。
答:需加水140 g
(2)设参加反应的氢氧化钾的质量为x,
HCl + KOH=KCl+H2O
36.5 56
7.3 g×2% x
36.5∶56="(7.3" g×2%)∶x x="0.224" g
废水中氢氧化钾的质量分数为
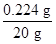 ×100%=1.12%
×100%=1.12%答:废水中氢氧化钾的质量分数为1.12%。

练习册系列答案
相关题目
