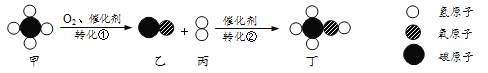
��Ŀ����
����Ŀ������������������ᷢչ�ļ�֤�ߣ����������ķ�չ�����Ľ���ͬ�������Ϲ�ϵʮ�����С�
��һ�������еĽ���
��1��û��þ�Ĵ��ڣ��Ͳ����γ�Ҷ���أ�Ҳ��û�й�����ã������þ��ָ_____��
A ���� B Ԫ�� C ԭ��
��2��������ˮƿ�ڵ��ϵ�����ɫ������_____����ͳѪѹ���еĽ���_____
��3��Ӳ����������dz����Ľ������ϡ���������_____��ѡ�����Ͻ�������������������
��4��Ϊ�˼��ٺͱ�����Ը߲㽨����Σ�����谲װ�ɽ��������Ƴɵı���װ�ã�����Ҫ�������˽������ϵ�_____��������ţ�
A �ܶȴ� B ������ C ������ D �۵��
������һ����̼��ԭ������
��ʵ��̽������ȤС���������ͼ��ʾʵ��װ�ý���ʵ�顣��24.0gij�������������ĩ���벣�����У���ַ�Ӧ�õ���ɫ�����ĩ����Ӧǰ��������װ�ú����ʵ������������������±���

��Ӧǰ | ��ַ�Ӧ�� | |
�� �� | �����ܺͺ�ɫ��ĩ��������Ϊ44.0g | �����ܺ������ʵ�������Ϊ36.8g |
�� �� | �Թܺ���ʢ��Һ��������Ϊ30.0g | ϴ��ƿ��ƿ������ ��������Ϊ32.1g |
���������ۣ�
��1��ʵ��ʱӦ��ͨCO���壬��������_____��
��2����ʵ��װ����һ���ԵIJ��ף�����Ϊ��_____��
��3��ʵ������Ӧ��ѡ��_____ ���ʵ�����ݼ�����ȷ����ɫ��ĩ�ijɷ֣���ѡ����һ���������_____����һ�㼴�ɣ������ռ����������������������ĩ�ۻ�ѧʽ��_____��
�������ɷַ���
���������ϣ���CO��ԭFe2O3�����Ĺ��̴��·�Ϊ�����Σ�
��1��3Fe2O3+CO![]() 2Fe3O4+CO2
2Fe3O4+CO2
��2��Fe3O4+CO![]() 3FeO+CO2
3FeO+CO2
��3��FeO+CO![]() Fe+CO2��
Fe+CO2��
�Ľ�����ʵ��װ�ã������¿ؼ���װ�ô���ƾ���̽��CO��һ��������������Ӧ������ʱ�����������¶ȱ仯��������ͼ��ʾ���ش��������⣺
��1���¶ȿ�����300������500����Χʱ����������û�з����仯��ԭ����_____��
��2��ͼ��H���Ӧ�Ĺ���ɷ���_____
��3��ͼ��M���Ӧa��������_____��
���𰸡�B Ag Hg �Ͻ� B �ž�װ���ڿ��������ⱬը ��β������װ�� �� ���ɵĶ�����̼û����ȫ������ Fe2O3 δ�ﵽ��Ӧ���������¶� ���������� 18g
��������
��һ�������еĽ���
1����������Ԫ����ɵģ�û��þ�Ĵ��ڣ��Ͳ����γ�Ҷ���أ�Ҳ��û�й�����ã������þ��ָþԪ�أ����B��
2��������ˮƿ�ڵ��ϵ�����ɫ�������������¼������Ľ����ǹ������Ag��Hg��
3��Ӳ��������ֱַ����������ĺϽ𣬲��Ǵ�����������Ͻ�
4������װ����Ϊ�˼��ٺͱ�����Ը߲㽨����Σ�����������˽������ϵĵ����ԣ����B��
������һ����̼��ԭ������
��1��һ����̼�Ϳ����Ļ�����ȼ���ܷ�����ը��������װ��A����ͨCO����������ǣ��ž�װ���ڿ��������ⱬը������ž�װ���ڿ��������ⱬը��
��2��ͼ1��ʾװ��û�ж�β�����д�����β���к����ж���һ����̼��ֱ���ŷ���ɿ�������Ⱦ�������β������װ�ã�
��3������ͨ��Һ��ʱ����Я��ˮ����������Ӧ��ѡ��I���ʵ�����ݼ�����ȷ����ɫ��ĩ�ijɷ֣���ѡ����һ��������ǣ����ɵ� ������̼û����ȫ�����գ��������ڹ�����ٵ�������Ϊ����������Ԫ�ص�������44.0g��36.8g��7.2g������Ԫ�ص�����Ϊ��24.0g��7.2g��16.8g����������������У���ԭ������ԭ�ӵĸ�����Ϊ��![]() ��
��![]() ��2��3�������������������������������ѧʽΪFe2O3������������ɵ� ������̼û����ȫ�����գ�Fe2O3��
��2��3�������������������������������ѧʽΪFe2O3������������ɵ� ������̼û����ȫ�����գ�Fe2O3��
�������ɷַ���
��1����ͼ���֪���¶ȿ�����300������500����Χʱ�������ﲻ����Ӧ���������¶ȣ�������������������δ�ı䡣���δ�ﵽ��Ӧ���������¶ȣ�
��2���������Ϣ�Լ�ͼ���֪��ͼ��H���Ӧ�����¶���600��������ɷ������������������������������
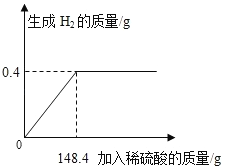
��3����ͼ���֪��M���Ӧ����700������������������������������ȫ������ʱ��������������Ϊ14.0g������������������Ϊx����
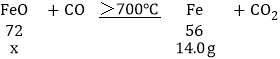
![]()
x��18g
���18g��

 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�����Ŀ���Ķ�������ն��ġ�
�����ij�����O3���ڳ�����������ɫ�����壬�����ŵ����ȳ�ζ�����ȶ�����ת��Ϊ����������Ȼ�ǿ��������������ἰ�Ĵ�����Ⱦ����������еij��������������ߣ������������ﲻ���˺������ҽ�����������Ӧ�÷�չ�Ͽ죬�������ǵ����ӡ�
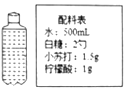
�����д���ʹ�õij���ͨ������ͼ��ʾ�����Ƶá�
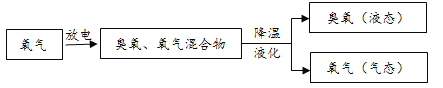
������������ˮ������19�������ڵ�ŷ�ޣ������ѱ���������ˮ���������ڳ�����ǿ�����ԣ�������ˮ�е��к����������Ǧ��������Ӧ������Ч���ã����������ζ��
������Ư���������л�ɫ�صķ�����������ᱻ�ƻ�����Ϊ��ɫ���ʡ���ˣ���������ΪƯ��������Ư���顢�ޡ�ֽ�ŵȡ�ʵ��֤����������Ư��������������15��֮�ࡣ
��������ҽ���������봫ͳ��������������ȣ������������ŵ㣬���1��ʾ��
��1 ��������������������Ա�
����Ч�� | ��������ʱ�䣨0.2mg/L�� | ������Ⱦ | Ͷ�ʳɱ� ��900m3�豸�� | |
���� | ��ɱ��һ���������ϸ����������ѿ�ߵ� | ��5min | �����ܿ�ת��Ϊ������������Ⱦ����Ч���� | Լ45��Ԫ |
���� | ��ɱ���ѿ������Ĵ��������Բ��������� | ��30min | �̼�Ƥ������������ζ���������к����ж�����Ⱦ���������ú������ˮ��ϴ | Լ3��4��Ԫ |
�����������ݻش��������⡣
��1��������O2���ͳ�����O3���е�Ƚϵ͵���_____��
��2��������������ˮʱ�������˳�����_____������������������ѧ�������ʡ�
��3�����ݱ�1��Ϣ��Ϊ�˿���ɱ����Ӧѡ�����������_____��
��4�����й��ڳ�����˵���У���ȷ����_____������ţ���
A ������Ư�����ñ�����ǿ
B �������Ƶó����Ĺ����У����������仯Ҳ�л�ѧ��
C �����������������кܶ���;��������������
D �����ȶ��Բ�����ڴ��棬��Ӧ�ÿ��ܻ��ܵ�����