��Ŀ����
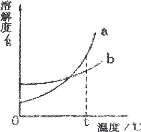
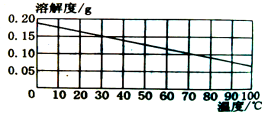
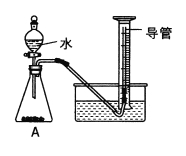
����Ŀ��С��ͬѧ��ʵ��������ȡCO2����Է�Һ���к���̽��������һ�������ĺ�CaCl2��HCl�ķ�Һ����μ���������������Ϊ10%��Na2CO3��Һ��ʵ������м���Na2CO3��Һ�����������������������������ϵ��ͼ1��ʾ������Na2CO3��Һ����������Һ��pH�仯��ϵ��ͼ2��ʾ������˵������ȷ����
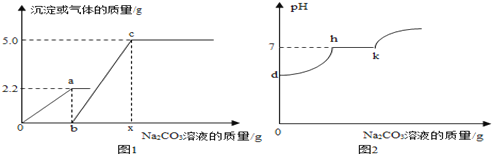
A. ͼ1��b��c�α�ʾ��������Ĺ���
B. ͼ1��b���ֵΪ106
C. ͼ1��c��ʱ����Һ�е�����������
D. ͼ1��0��a�η�Ӧ��������Һ��PH�仯�������ͼ2��d��h�����߱�ʾ
���𰸡�D
�����������������A��ͼ1��b��c�α�ʾ���ɳ����Ĺ��̣�����B��ͼ1��b��ʱ���ɶ�����̼2.2 g����μӷ�Ӧ��̼������Һ������Ϊx
Na2CO3+2HCl==2NaCl+CO2��+H2O
106 44
X��10% 2.2 g
106 : 44= X��10% ��2.2 g ���x="53" g ��B���� C��ͼ1��c��ʱ��̼�������Ȼ���ǡ�÷�Ӧ����Һ�е�����ֻ���Ȼ���һ�֣����� D��ͼ1��0��a�η�Ӧ��������Һ��PHһ��ʼС��7��������̼������Һʱ�����������٣�����������̼������Һ������ǡ�÷�ӦʱPH=7����D��ȷ����ѡD

��ϰ��ϵ�д�
�����Ŀ