题目内容
【题目】金属在生产和生活中有广泛的应用。
(1)下列金属制品中,利用金属导热性的是_____(填字母序号)。
A 灯泡中钨丝 B 铝导线 C 铁锅
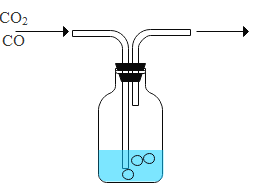
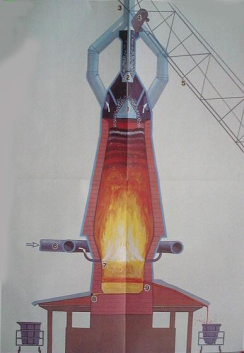
(2)我国之所以能在公元前6世纪就发明生铁冶炼技术,主要得益于我国很早就发明了比较强的鼓风系统和比较高大的竖炉(如下图)。该装置可用于一氧化碳还原赤铁矿(主要成分是氧化铁),写出炼铁反应的化学方程式____。
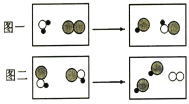
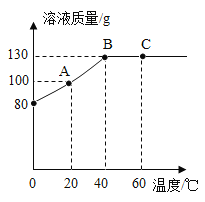
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如下图所示。下列说法正确的是____。
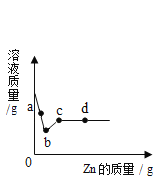
A a点溶液中溶质有2种
B c点溶液中溶质是Zn(NO3)2
C 若取b~c段固体,滴加稀盐酸,无气泡产生
D 取d点的固体有2种
【答案】C Fe2O3+3CO ![]() 2Fe+3CO2 BC
2Fe+3CO2 BC
【解析】
(1)A、灯泡中钨丝是利用钨的熔点高;
B、铝导线是利用金属导电性;
C、铁锅做饭是利用金属导热性。故选C;
(2)一氧化碳还原赤铁矿(主要成分是氧化铁)反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO ![]() 2Fe+3CO2;
2Fe+3CO2;
(3)在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
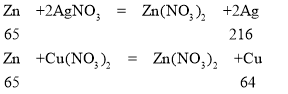
所以析出银的过程是溶液质量减少的过程,析出铜的过程是溶液质量增加的过程。
A、在a点时,硝酸银没有全部参加反应,故取a点溶液,溶质为Zn(NO3)2和Cu(NO3)2和AgNO3,故A错误;
B、c点时硝酸铜恰好完全反应,溶液中只有硝酸锌,故B正确;
C、b~c段是硝酸银全部参加反应完后锌和硝酸铜反应的过程,锌没有剩余,所以滴加稀盐酸,没有气泡,故C正确;
D、d点时锌过量,金属固体有锌、铜、银3种,故D错误。故选:BC。

练习册系列答案
相关题目