题目内容
【题目】化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①地壳中含量最高的非金属与金属元素组成的化合物________;
②两个氦原子________;
③三个二氧化硫分子________;
④四个铵根离子________。
(2)在符号“![]() ”中H正上方的“+1”表示__________,H右下角的“2”表示_________。
”中H正上方的“+1”表示__________,H右下角的“2”表示_________。
(3)“3Fe2+”中数字“3”表示___________右上角数字“2”表示____。
【答案】Al2O3 2He 3SO2 4NH4+ 水中氢元素的化合价为+1价 一个水分子中有2个氢原子 亚铁离子的个数为3个 每个亚铁离子带2个单位的正电荷
【解析】
(1)①地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝,氧化铝中铝元素显+3价,氧元素显-2价,其化学式为:Al2O3;
②根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,因此2个氦原子表示为:2He;
③由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则三个二氧化硫分子可表示为:3SO2;
④由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故四个铵根离子可表示为:4NH4+;
(2)标在元素符号正上方的数字表示该元素化合价的数值,标在化学式中元素右下角的数字表示一个分子中所含原子的数目,在符号“![]() ”中H正上方的“+1”表示水中氢元素的化合价为+1价、H右下角的“2”表示一个水分子中有2个氢原子;
”中H正上方的“+1”表示水中氢元素的化合价为+1价、H右下角的“2”表示一个水分子中有2个氢原子;
(3)离子符号前面的数字表示离子的个数,故“3”表示亚铁离子的个数为3个;元素符号右上角的数字表示离子所带的电荷数,故“2+”表示每个亚铁离子带2个单位的正电荷。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化作用呢?于是进行了以下探究。
(猜想)Ⅰ.CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后________。
(实验)用天平称量0.2 g CuO,取5 mL 5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_________,带火星的木条复燃 | _____________ | 溶液中有气泡放出,带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立 |
(2)步骤①的目的是___________。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学方程式为_____________。
【题目】金属材料广泛应用于生产生活中。
(l)铝块能制成铝箔是利用了铝的_________性(填“导电”或“延展”);铝的“自我保护”原因是___________。(用化学方程式表示)
(2)小张利用图示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略)
查阅资料:Fe3O4在常温下能与稀盐酸反应,方程式为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O,不与CuSO4溶液反应。
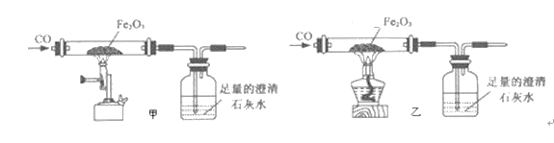
A.实验开始时应先通CO,目的是:___________;
B.从环保角度考虑,图示装置还应采取的改进措施是__________。
C.两实验过程中,澄清石灰水均变浑浊,发生的化学反应方程式为:_________,完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
2 | 取黑色粉末,加入稀盐酸 | 全部溶解,有大量气泡 | 无气泡产生 |
3 | 取黑色粉末,加入足量CuSO4溶液 | 有红色物质产生 | 无明显现象 |
①甲组的黑色粉末与稀盐酸反应的化学方程式是_________。
②根据实验现象,乙组实验玻璃管中发生的反应方程式为:__________。
③甲、乙两组实验说明温度对CO和Fe2O3反应____________(填有、无或不确定)影响。
(3)小兰对黄铜(Cu – Zn合金)中的Zn的含量进行了探究,将4.0g黄铜粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应,测得烧杯中剩余物质的质量为13.96g, 则:
①生成氢气的质量是_________g;
②若不考虑该合金中除Cu、Zn以外的其他成分,请计算原Cu – Zn合金中Zn的质量分数_______。(计算结果精确到小数点后一位)