题目内容
【题目】高纯氧化锌广泛应用于电子工业,某研究小组设计如图流程制备高纯氧化锌。
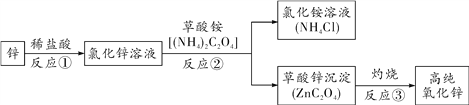
(1)反应①的化学方程式为________________________。
(2)反应②的基本反应类型是________________。
(3)反应②后进行的分离操作名称是________,若得到的NH4Cl溶液有浑浊,由于操作造成的原因可能是____________________(写出一种即可)。
(4)反应③属于分解反应,除得到氧化锌外还生成2种常见气体,其化学式为________、________。
【答案】 Zn+2HCl==== ZnCl2 +H2↑ 复分解反应 过滤 过滤时液面高于滤纸边沿 CO CO2
【解析】本题是流程题,研读流程图,从中获得解答题目所需的信息,在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息捕捉的有效性。
(1)锌与稀盐酸反应生成氯化锌和氢气,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑;
(2)由流程图和物质间的反应可知:②是氯化锌和草酸铵相互交换成分生成氯化铵和草酸锌沉淀,属于复分解反应;
(3)反应②后进行的分离操作名称是过滤,若得到的NH4Cl溶液有浑浊,原因可能是滤纸破损、液面高于滤纸边缘等;
(4)根据质量守恒定律,化学反应前后元素的种类和质量不变,反应③属于分解反应,草酸锌分解除了得到氧化锌外还生成CO2、CO。

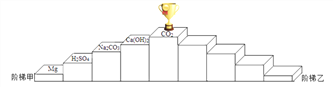
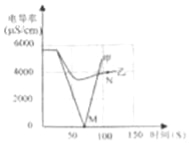
【题目】某同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如右图所示。

(1)该同学能收集到的二氧化碳的质量多少?(写出计算过程)
(2)该同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | 0 | 1 | n | 3 | 4 | 5 | m |
则m= 。加入10gNa2CO3溶液时发生反应的化学方程式是 。
请在右图中画出向废液中加入Na2CO3溶液时加入的Na2CO3溶液与产生的沉淀的曲线。

【题目】根据如表回答问题
温度(℃) | 20 | 40 | 50 | 60 | 80 | |
溶解度 (g/100g水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(1)50℃时,100g水中最多溶解NaCl______ g
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。

① A溶液为________(选填“饱和”或“不饱和”)溶液
② 对以下过程的分析,正确的是_________(选填编号)
a.A到B的过程中,溶质质量没有改变 b.B中溶质与溶剂的质量比为169:100
c.A溶液的质量等于222g d.开始析出KNO3固体的温度在60℃至80℃之间