题目内容
【题目】实验室制取气体所需装置如下图所示.
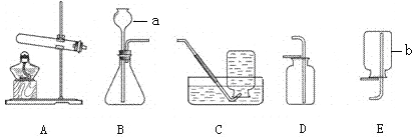
(1)实验仪器a、b的名称是a______、b_______.
(2)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____(填序号),其反应的化学方程式是______.
﹙3﹚用高锰酸钾制取氧气,其反应的化学方程式是______。试管口应放_______________。 实验结束,停止加热前要先将导管移出水面,目的是__________。
【答案】 长颈漏斗 集气瓶 B CaCO3+2HCl =CaCl2+H2O+CO2↑ 2KMnO4 ![]() K2MnO4+MnO2+O2↑ 棉花 防止水倒流引起试管炸裂
K2MnO4+MnO2+O2↑ 棉花 防止水倒流引起试管炸裂
【解析】(1)仪器a是长颈漏斗,仪器b是集气瓶;
(2)在常温下用大理石和稀盐酸来制取二氧化碳,因此不需要加热,属于固+液常温型,故选B装置;碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,化学方程式为: CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式为2KMnO4 ![]() K2MnO4 + MnO2 + O2↑;为防止高锰酸钾的固体小颗粒随气流进入导管,所以试管口应放棉团;实验结束,停止加热前要先将导管移出水面,再熄灭酒精灯,是为了防止水倒吸造成试管炸裂。
K2MnO4 + MnO2 + O2↑;为防止高锰酸钾的固体小颗粒随气流进入导管,所以试管口应放棉团;实验结束,停止加热前要先将导管移出水面,再熄灭酒精灯,是为了防止水倒吸造成试管炸裂。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下稀盐酸和氢氧化钙发生的中和反应实验探究。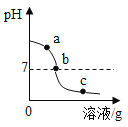
【演示实验】由图可知该实验操作是将______________滴加到另一种溶液中。该反应的化学方程式是___________________________;
【查阅资料】CaCl2溶液显中性, CaCl2+Na2CO3 =CaCO3↓+2NaCl
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2
猜想Ⅱ:有____________________
猜想Ⅲ:有CaC12和Ca(OH)2
猜想Ⅳ:有CaCl2、HC1和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是____________________________;
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊试液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | _______________ | ______________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想Ⅲ是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_______________________________;
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑________________。