��Ŀ����
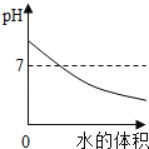
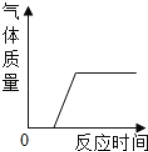
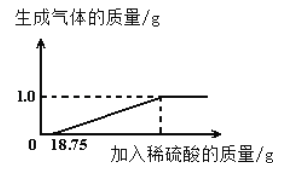
����Ŀ���ַ������Ȼ��ƺ��Ȼ�����ɵIJ�Ʒ���Ȼ��Ƶĺ�������ȡ13.4g������Ʒ��ȫ������96.6gˮ�У������õĻ����Һ�еμ�������������Ϊ10.6%��̼������Һ����¼����ͼ��ʾ�����߹�ϵ��
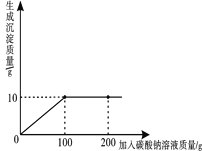
��1�����Ȼ�����̼����ǡ����ȫ��Ӧʱ������10.6%��̼������Һ��������_______g��
��2����Ʒ���Ȼ��Ƶ������Ƕ���_______��
��3�����Ȼ�����̼����ǡ����ȫ��Ӧʱ�����ˣ�������Һ�����ʵ����������Ƕ���_______��
���𰸡�100 2.3g 7%
��������
��1�������ɳ������������ߣ����Ȼ�����̼����ǡ����ȫ��Ӧʱ������10.6%��̼������Һ������Ϊ100g������̼��Ƶ�����Ϊ10g��
��2���裺��Ʒ���Ȼ��Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
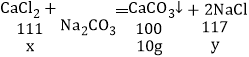
![]() x��11.1g��
x��11.1g��
![]() y��11.7g��
y��11.7g��
������Ʒ���Ȼ��Ƶ�������13.4g��11.1g��2.3g
��3��������Һ��������������=![]() ��
��
�𣺣�2����Ʒ���Ȼ��Ƶ�������2.3g��
��3��������Һ�����ʵ�����������7%��

 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�����Ŀ��Ϊ̽������Ļ�ѧ���ʣ�ij��ѧС����������ʵ�飺
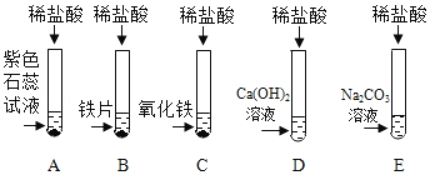
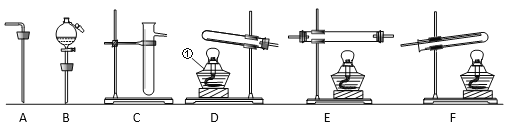
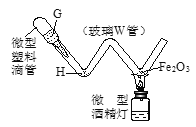
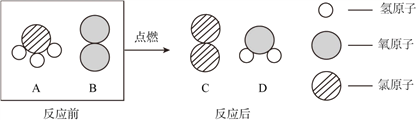
(1)A�Թ��е�ʵ������Ϊ_____��C�Թ�����������Ӧ�Ļ�ѧ����ʽΪ_____��
(2)����Ӧ��D��E�Թ��еķ�Һ����һ���ྻ���ձ��У��۲쵽�ձ����������ݲ��������а�ɫ�������֡����ձ��еĻ������ˣ��õ���ɫ��������ɫ��Һ��ͬѧ�Ƕ���Һ�����ʵijɷֽ���̽����
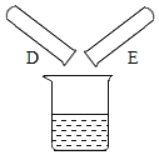
��������⣩��Һ�����ʵijɷ���ʲô��
���������룩���룺NaCl
�������NaCl��CaCl2
��������_____
�����ģ�NaCl��Ca(OH)2��HCl
���������ۣ��������ۣ�ͬѧ��һ����Ϊ����_____�Ǵ���ġ�
�����ʵ�飩�����ʵ�鱨�档
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ������Һ���Թ��У��μ�������̼������Һ�� | _____ | ����������� |
ȡ������Һ���Թ��У��μ�_____(������)�� | _____ | ���������� |
��Ǩ����չ��ϡ���ᡢϡ������һЩ���ƵĻ�ѧ���ʣ�����Ϊ�ڲ�ͬ������Һ�ж�����_____��