题目内容
【题目】某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取35g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示:
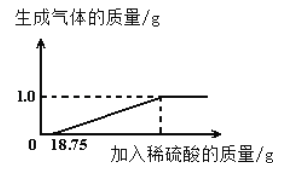
(1)产生氢气的质量为_______克。
(2)计算废铁锅片中单质铁的质量分数_______.(相对原子质量:Fe-56 H-1 S-32 O-16)
【答案】1.0 80%
【解析】
解:(1)由图可知,生成氢气的质量为1.0g
(2)设参加反应的铁电子的质量为x

56:2=x:1.0g
x= 28g
废铁锅片中单质铁的质量分数为![]() ×100%=80%
×100%=80%
答:(1)生成氢气的质量为1.0g;
(2)废铁锅片中单质铁的质量分数为80%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目