题目内容
【题目】火力发电厂(燃烧煤发电)会排放较多的二氧化硫,造成严重的环境问题是_____,该厂技术人员设计三种除硫环保方案:(已知亚硫酸钙不溶于水)
①用烧碱溶液吸收SO2,反应方程式是_____。
②用石灰浆(氢氧化钙的悬浊液) 反应方程式是_____。
③用石灰石浆吸收,反应方程式是2CaCO3+2SO2 +O2=2CaSO4+2CO2
(1)从降低成本的角度考虑,你认为最佳方案是_____(填方案序号)。
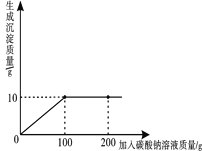
(2)若该发电厂排放的1000kg废气中含1.8kg的二氧化硫气体,计算除去4000kg废气中的二氧化硫至少需要含碳酸钙80%的石灰石多少kg_____?
【答案】酸雨; SO2+2NaOH=Na2SO3+H2O; Ca(OH)2+SO2═CaSO3↓+H2O; ③; 14kg。
【解析】
由于二氧化硫与水化合生成了酸,火力发电厂(燃烧煤发电)会排放较多的二氧化硫,造成严重的环境问题是酸雨;
由于二氧化硫能碱液反应生成了盐和水,所以:①用烧碱溶液吸收SO2,反应方程式是:SO2+2NaOH=Na2SO3+H2O.②用石灰浆(氢氧化钙的悬浊液) 反应方程式是:Ca(OH)2+SO2═CaSO3↓+H2O。
(1)由于氢氧化钠、氢氧化钙的成本较高,石灰石的成本较低,从降低成本的角度考虑,最佳方案是③。
(2)二氧化硫的质量为:1.8kg×![]() =7.2kg
=7.2kg
设至少需要含碳酸钙80%的石灰石的质量为x
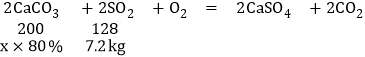
![]() 解得:x≈14kg
解得:x≈14kg

【题目】按要求回答下列各题。
(1)在下表空格中填写相应的化学式。
氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 |
KCl | CaCl2 | NaCl | _____ | AlCl3 | ZnCl2 | FeCl2 |
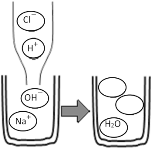
(2)如图表示稀盐酸和氢氧化钠溶液发生反应的微观过程,请你将如图空白圆圈中的离子符号填写到下面空格上_____、_______;请你说出盐酸与氢氧化钠反应的微观实质:____