题目内容
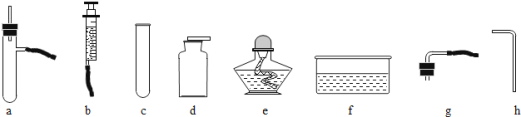
【题目】利用下列仪器进行实验(所有装置的气密性都已检查完毕)
(1)把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并收集氧气,完成该实验你所选用的仪器有__________(填字母)。写出发生反应的文字表达式____________________。这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有_______的优点。
(2)科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素。在四支试管中分别加入0.2克二氧化锰(MnO2)粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:
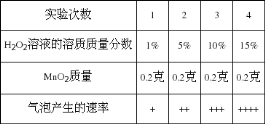
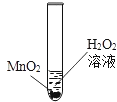
该实验研究的问题是,过氧化氢分解的速度与__________的关系。
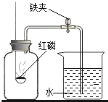
(3)某同学探究“红砖粉末是否也可以作过氧化氢分解反应的催化剂?”实验步骤和现象如下:
(4)
①他分别向两支试管中加入等质量等溶质质量分数的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快;
②将反应较快的试管内固体过滤出来,洗涤、烘干、称量;
③用称量后的固体重复步骤①的实验,现象与步骤①的完全相同。
(5)试回答:步骤①中他除了选用试管外,还应用到的仪器有_________ (填字母)步骤③的实验目的____________________.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来______________.
(6)为了检验产生的气体是否为氧气,请你写出检验方法____________________________.
(7)如图是实验室制取、收集有关气体的装置图,请按要求回答下列问题
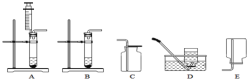
①要收集氧气,收集装置可选择上述装置中的 _____或D(填序列号)
②用D装置收集过程中,当氧气充满集气瓶后,将导管从瓶口处移开,________在桌上。
③用发生装置A或B制取氧气时,A与B相比,A的优点是____________________.
④实验室制取二氧化碳组装仪器时连接玻璃管和橡皮管的方法是先把玻热管口_______然后稍稍用力即可把玻璃管插入胶皮管。
(8)该小组设计了如图所示实验装置,既可用于制取气体,又可用于探究物质性质。
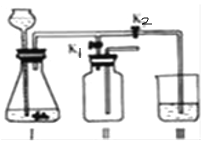
①当打开K1,关闭K2时,利用Ⅰ、Ⅱ装置,可进行的实验是________(填字母)。
a.石灰石与稀盐酸反应制取二氧化碳
b.块状锌粒与稀硫酸反应制取氢气
②当打开K2,关闭K1时,可以利用I、III装置制得二氧化碳并验证其性质。实验室制取二氧化碳的文字表达式是______;若要证明二氧化碳与水反应,应向烧杯中加入____。
【答案】a、b、d、h双氧水![]() 水+氧气可控制反应速率H2O2溶液的溶质质量分数f、g、h检验红砖粉末实验前后的质量和化学性质是否改变实验开始前未称量红砖粉末质量将带火星的木条放在导管口,若木条复燃则为氧气C正放可以控制反应速率润湿B稀盐酸+石灰石→氯化钙+水+二氧化碳紫色石蕊试液
水+氧气可控制反应速率H2O2溶液的溶质质量分数f、g、h检验红砖粉末实验前后的质量和化学性质是否改变实验开始前未称量红砖粉末质量将带火星的木条放在导管口,若木条复燃则为氧气C正放可以控制反应速率润湿B稀盐酸+石灰石→氯化钙+水+二氧化碳紫色石蕊试液
【解析】
(1)制取氧气需要试管和添加反应物的注射器,收集氧气需要集气瓶和导管,故填a、b、d、h;过氧化氢在二氧化锰的催化作用下能分解生成水和氧气,反应的文字表达式为:双氧水![]() 水+氧气;使用注射器添加双氧水,能控制反应的速率,得到平稳的气流,可以随时停止,有利于节约药品;
水+氧气;使用注射器添加双氧水,能控制反应的速率,得到平稳的气流,可以随时停止,有利于节约药品;
(2)根据表格可知,加入二氧化锰质量相同,过氧化氢浓度不同,故该实验研究的问题是过氧化氢分解的速度与H2O2溶液的溶质质量分数的关系;
(5)步骤①中他除了选用试管外,还应用到的仪器有橡胶塞、玻璃导管和盛有水的水槽,故填f、g、h;步骤③的实验目的检验红砖粉末实验前后的质量和化学性质是否改变;催化剂要符合反应前后质量和化学性质均不变,故该同学的实验还缺少一个关键步骤,实验开始前未称量红砖粉末质量;
(6)检验氧气的方法为:将带火星的木条放在导管口,若木条复燃则为氧气;
(7)
①氧气的密度大于空气,不易溶于水,可采用向上排空气法或者排水法收集氧气,故收集装置可选择上述装置中的C或D;
②当氧气充满集气瓶后,将导管从瓶口处移开,氧气的密度大于空气,为了防止氧气逸出,要将集气瓶正放在桌上;
③用发生装置A或B制取氧气时,A与B相比,A的优点是可以控制反应速率;
④连接玻璃管和橡皮管的方法是先把玻热管口润湿,然后稍稍用力即可把玻璃管插入胶皮管。
(8)
①集气瓶中可收集密度小于空气的气体,故可进行的实验是b.块状锌粒与稀硫酸反应制取氢气;
②实验室利用大理石或者石灰石与稀盐酸反应制取二氧化碳,生成氯化钙、水和二氧化碳,其文字表达式为稀盐酸+石灰石→氯化钙+水+二氧化碳;若要证明二氧化碳与水反应,应向烧杯中加入紫色石蕊试液。

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案【题目】某食品的包装袋中放有一小包“防腐剂”,化学兴趣小组的同学对“防腐剂”的成分产生了好奇,他们将一包“防腐剂”倒在滤纸上,看到“防腐剂”中有一些灰黑色粉末和一些红色粉末,为此,展开以下探究活动:
(提出问题)“防腐剂”中灰黑色的粉末和红色的粉末分别是什么?
(查阅资料)食品腐败主要是因为食品易被空气中的氧气和水蒸气氧化、潮解而变质,使用“防腐剂”可延长食品的保质期;氧化铁可与稀盐酸反应生成氯化铁和水,其溶液因电解出铁离子而呈黄色。
(提出猜想)小明:“防腐剂”中灰黑色的粉末是氧化铜,红色的粉末是铜。
小红:“防腐剂”中灰黑色的粉末是氧化铜和碳粉,红色的粉末是铜。
小军:“防腐剂”中灰黑色的粉末是铁粉和碳粉,红色的粉末是氧化铁。
(讨论分析)通过讨论,同学们一致认为小军的猜想是正确的。理由是:_______________________。
(实验探究)请你参与他们的探究,并将实验内容补充完整。
实验步骤及操作 | 实验现象 | 实验结论 |
用磁铁接近滤纸上的“防腐剂”,并充分吸引。 | 磁铁上吸引 了部分黑色物质 | ___________________ |
② 取①中剩余的粉末于试管中,加入足量的_________,观察现象。 | _________________________________ | 小军猜想成立,写出化学 方程式: _________________________ |
(拓展探究)为了进一步探究“防腐剂”的性质,兴趣小组的同学另取一包“防腐剂”粉末装入硬质玻璃管中,进行了如图所示的实验。
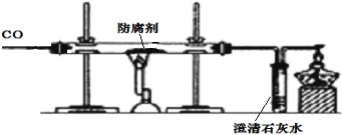
(1)该实验表现出CO具有的化学性质是___________________________。其实际操作中用量比理论值大的原因是____________________________________________。
(2)实验结束后,通过称量反应前后硬质玻璃管中固体物质的质量,他们发现反应后红色固体物质变成黑色而且的质量减小,质量减小的原因______________________。
【题目】去年6月5日世界环境日的主题为:“水--20亿人生命之所系”,请你参与下列问题的讨论。
(1)净水过程中,利用活性炭的________作用同时除去臭味和一些溶解的杂质。
(2)去年9月份,南京城北污水处理系统一期工程如期完成.届时湖南路、中山路、新模范马路及下关部分地区的水环境将首先得到改善,为了检测废水是否达到排放标准,请你设计以下实验:在实验室过滤除去废水中的固体杂质,所需的玻璃仪器有________、________、________。
(3)三峡工程(二期)已于2003年6月1日开始蓄水,为防止三峡库区水被污染,应采取的措施是(填序号)________。
①清理蓄水库库底固体废物 ②防治船舶污染 ③整治相关河流污染 ④治理库区和上游工业污染区
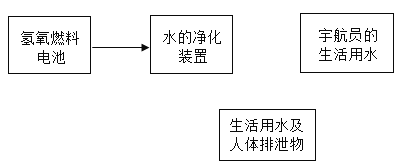
(4)载人飞船必须建立水的循环体系,以保证宇航员的生活用水,并减少飞船的携水量.请将下图各项用箭头连接成水的循环体系_______。(注:氢氧燃料电池反应产生电能,同时生成水)
(5)根据下面两张图表提供的有关数据,北京水资源紧缺指标属于________范围。所以,我们每个北京市民都必须爱护水资源;一方面要防止水体污染,另一方面要________用水,图是我国各地区(香港、澳门、台湾暂未列入)人均水量。
图表:水资源紧缺指标
紧缺性 | 轻度缺水 | 中度缺水 | 重度缺水 | 极度缺水 |
人均水量m3/年 | 17003000 | 10001700 | 5001000 | <500 |

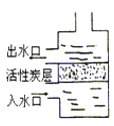
下图是市场上出售的一种活性炭净水器示意图,这种净水器可以除去水中的难溶________。
(6)自然界中采集到的湖水、河水的水样,一般比较浑浊,可通过(填一种操作方法)________的方法,得到较澄清的水样。
(7)硬水和软水的本质区别是________含量的多少不同,家庭生活中可以用________检验某水样是硬水还是软水。
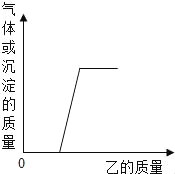
【题目】向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用如图曲线表示的是( )
序号 | 甲 | 乙 |
① | HNO3和Mg(NO3)2的混合溶液 | KOH溶液 |
② | Ag﹣Zn合金 | 稀H2SO4 |
③ | 久置空气中的铝片 | 稀盐酸 |
④ | 含有Na2CO3的NaOH溶液 | 稀HNO3 |
⑤ | HCl和H2SO4的混合酸 | Ba(NO3)2溶液 |
A. ②⑤ B. ①③④ C. ①②④ D. ①③⑤