题目内容
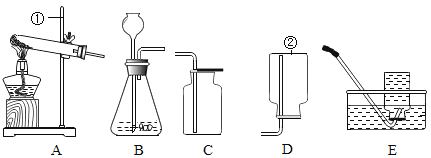
【题目】如图常见实验装置,请根据要求填空.(填写装置编号①--⑦,有先后顺序,装置可重复使用假设每步反应都完全)

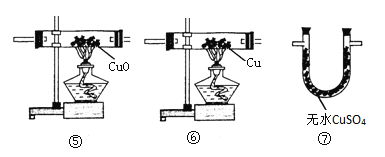
(1)除去N2中的水蒸气和二氧化碳选用装置的顺序为_____;
(2)除去用浓盐酸和石灰石制得的CO2中的杂质,选用装置的顺序为_____,其中气体与瓶中试剂发生反应的方程式_____,实验室制取CO2的方程式_____;
(3)检验N2中的H2和水蒸气,选用装置的顺序为_____。
【答案】①② ④② NaHCO3+HCl=NaCl+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ ⑦⑤
【解析】
(1)除去空气中的水蒸气和二氧化碳,可以使用氢氧化钠溶液和浓硫酸,需要先除去二氧化碳后进行气体的干燥,这两个过程都需要导气管底进上出,并且底进的导气管要插入液体中,故填:①②;
(2)盐酸具有挥发性,用浓盐酸和石灰石制得的CO2中的杂质是氯化氢和水蒸气。若要除去CO2中混有的HCl气体和水蒸气,得到纯净的CO2,应在收集装置前连接两个装置,在第一个装置中放入足量的NaHCO3溶液,是除去氯化氢气体的;第二个装置中放入足量的浓硫酸是除去水蒸气,要先除杂质再干燥;氯化氢溶于水形成盐酸,盐酸与碳酸氢钠反应生成氯化钠、水和二氧化碳;石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;故填:④②;NaHCO3+HCl=NaCl+H2O+CO2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)氢气具有还原性,在加热的条件下,能将氧化铜还原为红色的金属铜,同时生成水,水蒸气能使白色的无水硫酸铜粉末变成蓝色;所以先将气体通过装置⑦来检验水蒸气的存在,然后再通过装置⑤,通过观察黑色粉末是否变成红色来判断是否存在氢气;故填:⑦⑤。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】某小组对测定空气中氧气体积分数的实验进行了如下研究
(1)选用汞、磷、铜等物质均可以完成该实验,选择反应物的依据是________________.
a、反应物是固体b、在空气中反应且只消耗氧气
c、燃烧有明显现象d、生成物不是气体
(2)用甲、乙两套装置进行实验(红磷充足、装置不漏气).红磷燃烧的化学方程式是________________,有关分析合理的是________________.
a、都只能在实验结束后,推得氮气是无色气体
b、甲中燃烧匙伸入集气瓶太慢,测得空气中氧气的体积分数将偏大
c、乙中的瘪气球可以防止燃烧放热使橡胶塞弹出
d、乙比甲更节约能源
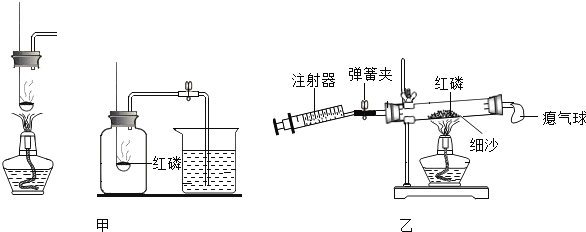
(3)利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹.反应前后各数据及结论如下.
玻璃管中原有 空气的体积 | 注射器中气体的体积 | 结论 | |
反应前 | 反应后 | ||
________mL | 40ml | 30ml | 氧气约占空气体积的五分之一 |
(4)乙装置气密性检查方法________________________
(5)注射器中气体最好是________________。按理论值计算,反应后注射器中气体体积应该(填大于、小于、等于____________30ml
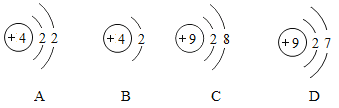
【题目】下表是元素周期表中第2、3周期的元素,请回答有关问题。
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)下列各组具有相似化学性质的元素是________________(填字母序号);
A. Na、Cl B.O、S C. F、Cl D. Cl、Ar
(2)写出一条第三周期元素原子的核外电子排布规律______________________________________________;
(3)第7号元素与第12号元素的原子形成化合物的化学式为_____________;
(4)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体是________________(填字母序号)。
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43和SO42
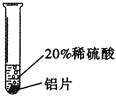
【题目】小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动。
(查阅资料)铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液……
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
(预 测)三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
(实验过程)取大小相同的三种金属薄片,用砂纸打磨光亮。
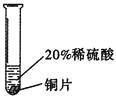
实验一 | 实验二 | 实验三 | |
实验 |
|
|
|
实验 | 铬片表面产生气泡 | _____________________ | 铝片表面产生气泡较快。 |
结论 | 铬能和稀硫酸发生 | 铜不与稀硫酸反应 | ____________________ |
三种金属在金属活动性顺序中的相对位置关系是 | |||
(回答问题)
(1)用砂纸打磨金属片的目的是_____________________。
(2)实验一所发生反应的化学方程式是 。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是 。
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是 。