题目内容
【题目】某小组对测定空气中氧气体积分数的实验进行了如下研究
(1)选用汞、磷、铜等物质均可以完成该实验,选择反应物的依据是________________.
a、反应物是固体b、在空气中反应且只消耗氧气
c、燃烧有明显现象d、生成物不是气体
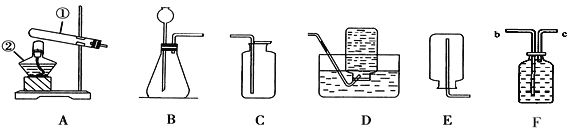
(2)用甲、乙两套装置进行实验(红磷充足、装置不漏气).红磷燃烧的化学方程式是________________,有关分析合理的是________________.
a、都只能在实验结束后,推得氮气是无色气体
b、甲中燃烧匙伸入集气瓶太慢,测得空气中氧气的体积分数将偏大
c、乙中的瘪气球可以防止燃烧放热使橡胶塞弹出
d、乙比甲更节约能源
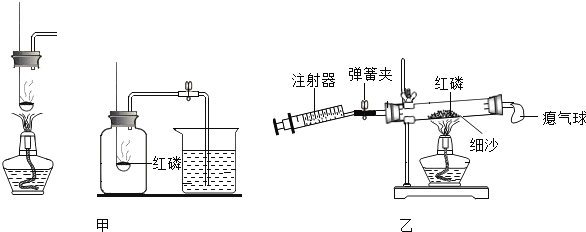
(3)利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹.反应前后各数据及结论如下.
玻璃管中原有 空气的体积 | 注射器中气体的体积 | 结论 | |
反应前 | 反应后 | ||
________mL | 40ml | 30ml | 氧气约占空气体积的五分之一 |
(4)乙装置气密性检查方法________________________
(5)注射器中气体最好是________________。按理论值计算,反应后注射器中气体体积应该(填大于、小于、等于____________30ml
【答案】bd 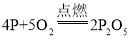 bc 50mL 打开弹簧夹,向右推动注射器活塞,右侧的气球胀大,一段时间后不缩小,证明装置严密 氮气 小于
bc 50mL 打开弹簧夹,向右推动注射器活塞,右侧的气球胀大,一段时间后不缩小,证明装置严密 氮气 小于
【解析】
红磷燃烧生成五氧化二磷。
(1)选用汞、磷、铜等物质均可以完成测定空气中氧气体积分数的实验,选择反应物的依据是在空气中反应且只消耗氧气、生成物不是气体,故选bd。
(2)红磷燃烧生成五氧化二磷,反应的化学方程式是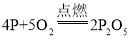
a、氮气是无色气体,在实验前后均是,故a不正确;
b、甲中燃烧匙伸入集气瓶太慢,空气逸出,测得空气中氧气的体积分数将偏大,故b正确;
c、乙中的瘪气球可以防止燃烧放热使橡胶塞弹出,故c正确;
d、甲比乙更节约能源,故d不正确。故选bc。
(3)利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹,注射器中气体的体积反应前40mL,反应后30mL,消耗了10 mL,氧气约占空气体积的五分之一,故玻璃管中原有空气的体积为![]()
玻璃管中原有 空气的体积 | 注射器中气体的体积 | 结论 | |
反应前 | 反应后 | ||
50mL | 40mL | 30mL | 氧气约占空气体积的五分之一 |
(4)乙装置气密性检查方法打开弹簧夹,向右推动注射器活塞,右侧的气球胀大,一段时间后不缩小,证明装置严密。
(5)氮气不活泼,故注射器中气体最好是氮气;按理论值计算,反应后注射器中气体体积应该小于30mL,因为氧气的理论值是21%;故按理论值计算,反应后注射器中气体体积应该小于30mL。

【题目】某国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表:(假设纸张其他成分既不溶于水,也不与水反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成 气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(1)表中X的值为;______
(2)求样品中碳酸钙的质量分数;_____
(3)计算所用稀盐酸溶质的质量分数?_______
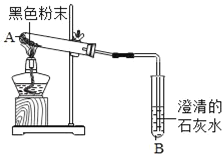
【题目】两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想)甲同学:A是铁粉,B是二氧化锰.乙同学:A是炭粉,B是氧化铜.
(查阅资料)碳粉和二氧化锰均不能与稀硫酸反应:而CuO+H2SO═CuSO4+H2O.
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是_____. |
②取少量B粉末于试管中,加入适量稀硫酸. | _____ | B粉末是氧化铜. |
(反思与拓展)
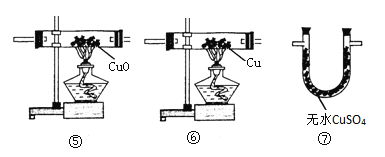
③将这两种黑色粉末混合加热(如图),试验中观察到的现象是_____.
④A中发生反应的化学方程式为_____.
②实验结束时,撤导管和熄灭酒精灯的顺序为先_____.
(结论)_____同学的猜想正确.