题目内容
【题目】某同学为了制作“叶脉书签”需要100g溶质质量分数为10%的氢氧化钠溶液。请问:
(1)需要氢氧化钠固体的质量是_________g.
(2)若用20%的氢氧化钠溶液来配制上述的氢氧化钠溶液,需要20%的氢氧化钠溶液质量__g.
(3)若该同学想把制作“叶脉书签”的氢氧化钠溶液处理掉,用50g稀硫酸怡好把碱液完全中和.试计算反应后溶质的质量分数?___(结果保留一位小数)
【答案】10 50 11.8%
【解析】
解:(1)100g溶质质量分数为10%的氢氧化钠溶液所含氢氧化钠固体的质量是100g×10%=10g;
(2)若用20%的氢氧化钠溶液来配制上述的氢氧化钠溶液,根据溶液稀释过程中溶质的质量不变可求需要20%的氢氧化钠溶液质量:![]() =50g;
=50g;
(3)设反应后溶质的质量分数为x,
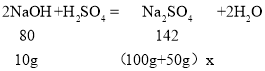
![]()
x≈11.8%;
答:(1)需要氢氧化钠固体的质量是 10g;
(2)若用20%的氢氧化钠溶液来配制上述的氢氧化钠溶液,需要20%的氢氧化钠溶液质量 50g;
(3)反应后溶质的质量分数为11.8%。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想)甲同学:A是铁粉,B是二氧化锰.乙同学:A是炭粉,B是氧化铜.
(查阅资料)碳粉和二氧化锰均不能与稀硫酸反应:而CuO+H2SO═CuSO4+H2O.
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是_____. |
②取少量B粉末于试管中,加入适量稀硫酸. | _____ | B粉末是氧化铜. |
(反思与拓展)
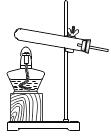
③将这两种黑色粉末混合加热(如图),试验中观察到的现象是_____.
④A中发生反应的化学方程式为_____.
②实验结束时,撤导管和熄灭酒精灯的顺序为先_____.
(结论)_____同学的猜想正确.

【题目】实验室制取气体常用的发生装置和收集装置如下表。
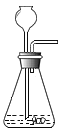
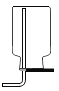
气体发生装置 |
|
|
|
A | B | C | |
气体收集装置 |
|
|
|
D | E | F |
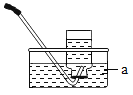
(1)写出装置图中标号仪器的名称:a____________。
(2)实验室用过氧化氢溶液制取氧气的化学方程式为_____________。下列混合过氧化氢溶液和二氧化锰的方法中,方法__________(选填“一”或“二”)可以得到平稳的氧气流。
方法一:把二氧化锰加入装有过氧化氢溶液的试管中
方法二:把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
(3)实验室用高锰酸钾制取氧气的化学方程式为______________。可选用D作为氧气的收集装置,原因是________________;若选用F作为氧气的收集装置,当_________时,再把导管口伸入盛满水的集气瓶。
(4)利用收集的氧气,验证氧气的性质。
①铁丝在氧气中燃烧。

该反应的化学方程式为______________。集气瓶中预先加有少量水,作用是________________。
②木炭在氧气中燃烧。

木炭在空气中燃烧的现象 | 木炭在氧气中燃烧的现象 | |
不同点 | ___________________ | _________________ |
相同点 | 放出___________,生成能使澄清石灰水___________的气体 | |