题目内容
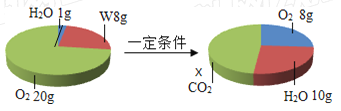
【题目】将乙醇和氧气置于密闭容器中引燃,测得反应前后各物质的质量如下:
物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量 | 未知1 | 未知2 | 0 | 0 | 0 |
反应后质量 | 0 | 0 | | | 待测 |
未知2和待测的值分别是______、______;写出该反应的化学方程式______。
【答案】4.0g 1.4g ![]()
【解析】
根据化学反应前后元素质量不变可得,水中的氢元素全部来自于乙醇中,则有水中氢元素的质量![]() ,氧元素的质量为
,氧元素的质量为![]() 根据物质质量等于元素质量除以元素质量分数可得,乙醇的质量为:
根据物质质量等于元素质量除以元素质量分数可得,乙醇的质量为:![]() ,则碳元素的质量为:
,则碳元素的质量为:![]() ,则氧元素质量
,则氧元素质量![]() ,因为乙醇中的碳转化到了一氧化碳和二氧化碳中,二氧化碳中碳元素的质量
,因为乙醇中的碳转化到了一氧化碳和二氧化碳中,二氧化碳中碳元素的质量![]() ,氧元素的质量为
,氧元素的质量为![]() ,一氧化碳中碳元素的质量
,一氧化碳中碳元素的质量![]() ,根据物质质量等于元素质量除以元素质量分数的一氧化碳的质量为:
,根据物质质量等于元素质量除以元素质量分数的一氧化碳的质量为:![]() ,则氧元素的质量为
,则氧元素的质量为![]() ,综上所示,乙醇的质量为
,综上所示,乙醇的质量为![]() ,氧气的质量为:
,氧气的质量为:![]() ,二氧化碳的质量为
,二氧化碳的质量为![]() 。一氧化碳的质量为
。一氧化碳的质量为![]() ,水的质量为
,水的质量为![]() 。可知乙醇和氧气点燃条件下生成二氧化碳和水、一氧化碳,反应方程式为:
。可知乙醇和氧气点燃条件下生成二氧化碳和水、一氧化碳,反应方程式为:![]() 。
。

练习册系列答案
相关题目