题目内容
【题目】如图是工业上在一定条件下制取乙醇反应的微观示意图![]() 其中“
其中“![]() ”代表氢原子,“
”代表氢原子,“![]() ”代表碳原子,“
”代表碳原子,“![]() ”代表氧原子
”代表氧原子![]() 。下列叙述不正确的是( )
。下列叙述不正确的是( )
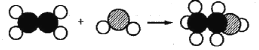
A. 反应物均为化合物
B. 反应前后三种物质的分子个数比为1:1:1
C. 乙醇中碳、氢、氧三种元素的质量比为12:3:8
D. 1个乙醇分子由1个氧原子、2个碳原子、3个氢分子构成
【答案】D
【解析】
据图可以看出,该反应是![]() ,
,
A、由微粒的构成可知,反应物均为由不同元素组成的纯净物,是化合物,故选项正确;
B、据质量守恒定律可知,反应前后各原子的种类、个数相等,故反应前后三种物质的分子个数比为1:1:1,说选项正确;
C、乙醇的化学式为![]() ,其中碳、氢、氧三种元素的质量比为
,其中碳、氢、氧三种元素的质量比为![]() :
:![]() :
:![]() 12:3:8,故选项正确;
12:3:8,故选项正确;
D、乙醇的化学式为![]() ;1个乙醇分子由1个氧原子、2个碳原子、6个氢原子构成,乙醇分子中不含有氢分子,故选项错误。
;1个乙醇分子由1个氧原子、2个碳原子、6个氢原子构成,乙醇分子中不含有氢分子,故选项错误。
故选:D。

练习册系列答案
相关题目
【题目】将乙醇和氧气置于密闭容器中引燃,测得反应前后各物质的质量如下:
物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量 | 未知1 | 未知2 | 0 | 0 | 0 |
反应后质量 | 0 | 0 | | | 待测 |
未知2和待测的值分别是______、______;写出该反应的化学方程式______。