��Ŀ����
����Ŀ����Ȼ����Ϊ�����Դ�ѳ�Ϊ�ҹ��ִ������е���ѡȼ�ϣ�LNG���ǵ���������Ȼ����ר�ô���������Ϊ�����촬���ʹ��ϵ���������ij��ȤС���ͬѧΧ���Ŵ���ʹ�õĽ������Ͻ������о���
��1���ں��Ӳ���ֹܵ�ʱ��ͨ��Ҫʹ���������������������Ϊ����Ļ�ѧ����_________��
��2�������ں�ˮ�������ⸯʴ���������õ�����ɫ�Ĺ��壩���촬��ҵΪ�˱����ִ��ĸ�����DZ���ʴ��ͨ�����ִ������Ƕ����һ�ֽ��������øý��������Ļ�ԵIJ�ͬ�����������ױ���ʴ��
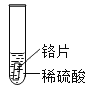
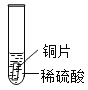
���о�����1��һ������£����ֻ�Բ�ͬ�Ľ����ڳ�ʪ�Ļ����нӴ�ʱ�����ֽ����ȱ���ʴ�أ�
��ʵ�����1������ĥ��Ľ���Ƭ������ͼ��ʾ��ʵ�飬
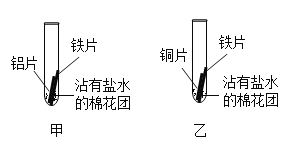
����һ��ʱ��۲쵽�������������±���
���� | ���� |
���У���Ƭ������ֻҰ�ɫ���ʣ���Ƭ���漸��û���������� | �������ڳ�ʪ�Ļ����нӴ��������ȱ���ʴ�� |
���У���Ƭ�������___________��ͭƬ���漸��û���������� | ����ͭ�ڳ�ʪ�Ļ����нӴ��������ȱ���ʴ�� |
���ó����ۣ�һ������£����ֻ�Բ�ͬ�Ľ����ڳ�ʪ�Ļ����нӴ�ʱ����Խ�___________������ǿ�������������Ľ������ȱ���ʴ��
��֪ʶӦ�ã��촬��ҵΪ�����ִ��ĸ�����DZ���ʴ��ͨ�����ִ������Ƕ�Ľ�����_____�����ţ�
A ���� B ͭ�� C ���� D п��
��3��LNG����ʹ���˴�����пͭ�Ͻ�
���о�����2���ⶨпͭ�Ͻ���п��ͭ����������
��ʵ�����2��������ͼ��ʾ��ʵ�顣
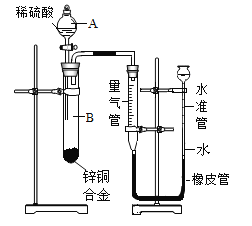
��ͼ�������ܺ�ˮ�ܿ������������������Ϊȷ����������������ڶ�ȡ��������Һ������Ĺ����У�Ӧע��________������ĸ����
A ����ʱ�����밼Һ����ʹ���ƽ
B ����ǰӦ�����ƶ�ˮ�ܣ�������Һ����ƽ�ٶ���
C ����ˮ�ܾ�ֹ����ˮ����Һ�治������ʱ�ٶ���
��ʵ��ǰ�����Ѿ���ĥ���Ŀ�״пͭ�Ͻ�ӹ�����м����Ŀ���ǣ�________��
��ʵ��������裺��������ԣ���ҩƷ��ˮװ��������У����Ӻ�װ�ú��ٴμ��װ�õ������ԣ���¼�����ܵ�Һ��λ��Ϊ5mL����A��B�μ������Լ�����B�в���������������ָ������º�¼�����ܵ�Һ��λ��Ϊ85mL����B��ʣ�������ˣ�ϴ�ӣ�����õ�����ƽ��������Ϊ0.416�ˡ�
�����ݴ�������ʵ�������£��������ܶ���0.09gL-1���������������ݼ���пͭ�Ͻ���ͭ����������_______������д��������̣�
������������������淶��������ȷ����ͨ�������������ͭ��������������ֵ���ǵ�����ʵֵ������Ҫԭ���ǣ�____________��
���𰸡��ȶ� ����ɫ���� ǿ D AB �����ϡ����ĽӴ�������ӿ췴Ӧ�ٶ� 64% �����ϡ����ռ��һ�������
��������
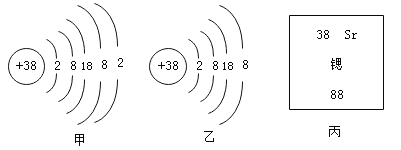
(1)��Ϊ�ԭ�ӵ�����������Ϊ8���ﵽ���ȶ��ṹ����ˣ����ԭ�ӹ��ɵ������ѧ�����ȶ�������д���ȶ���
(2)���У����ȱ���ʴ���������������ı�����ֺ���ɫ���壻�ʴ𰸣�����ɫ���壻
(3)���ݽ������˳�����֪�����������ã�����ͭ���ã�һ������£����ֻ�Բ�ͬ�Ľ����ڳ�ʪ�Ļ����нӴ�ʱ����Խ�ǿ�Ľ����ȱ���ʴ������д��ǿ��
(4)��(3)������֪��Ҫѡ�ý�����Ա���ǿ�Ľ���п���ʴ𰸣�D��
(5)����ʱ��Ҫע������Ӧ�������ܰ�Һ�����ʹ�����ˮƽ��ÿ�ζ���ǰӦ�����ƶ�ˮ�ܣ�������Һ����ƽ�ٶ�������Ϊ�˷�ֹˮ��ѹǿ��ɵ�����ѡAB��
(6)пͭ�Ͻ�ӹ�����м����ϡ����ĽӴ���������Լӿ췴Ӧ�ٶȣ��ʴ𰸣������ϡ����ĽӴ�������ӿ췴Ӧ�ٶȣ�
(7)ͭп�Ͻ���ϡ���ᷴӦ�������������85mL-5mL=80mL��������������=0.080L��0.09g/L=0.0072g��
�⣺���ϡ���ᷴӦ�ĺϽ���п������Ϊx
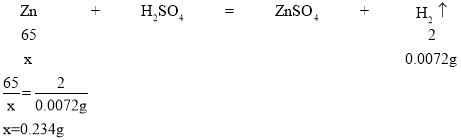
�Ͻ������Ϊ0.234g+0.416g=0.65g
���ԣ��Ͻ���ͭ����������![]() ��100%=64%
��100%=64%
�����64%��
(8)��������ʵ��װ�ã���������ܻ�ƫС��ԭ���Ǽ����ϡ����ռ��һ�������
��

����Ŀ��С���뵽�����»���ˮ��ͷ����˵�������˽��ˮ��ͷ��ͭ�ʶƸ��������С����̽������Cr���볣����������ͭ�Ļ��ǿ����������һͬ�μӡ�
��֪ʶ�طţ�
�������˳��K Ca Na MgAl Zn Fe Sn Pb ��H�� Cu_____Ag Pt Au�������ں�������д��Ӧ������Ԫ�ط��š�
���������룩
����1.Cr>Fe>Cu�� ����2. Fe>Cu >Cr�� ����3.��IJ�����__________��
���������ϣ�
��1����������ɫ�й���Ľ������ڿ���������������ɿ���ʴ����������Ĥ��
��2��������ϡ���ᷴӦ��������ɫ�������Ǹ���CrSO4����Һ��
�������ʵ�飩
С��ͬѧȡ��С��ȵ����ֽ���Ƭ����ɰֽ��ĥ��������ȡ��֧�Թܣ��ֱ���������ͬ��ϡ���ᡣ
ʵ�� | �Թ�1 | �Թ�2 | �Թ�3 |
ʵ�� ���� |
|
|
|
ʵ�� ���� | ��Ƭ����������ݽ�������Һ��Ϊdz��ɫ | ��Ƭ����������ݽϿ죬��Һ���Ϊ��ɫ | ________ |
����������ͣ�
��1��С�ϵõ��Ľ����Dz���__________��ȷ��
��2��ʵ��ǰ��ɰֽ��ĥ����Ƭ��Ŀ����_______________��
��֪ʶ���ã�����ƬͶ��FeSO4��Һ�У���Ӧ__________�������������������������С����ܽ��У�����д����Ӧ�Ļ�ѧ����ʽ____________��